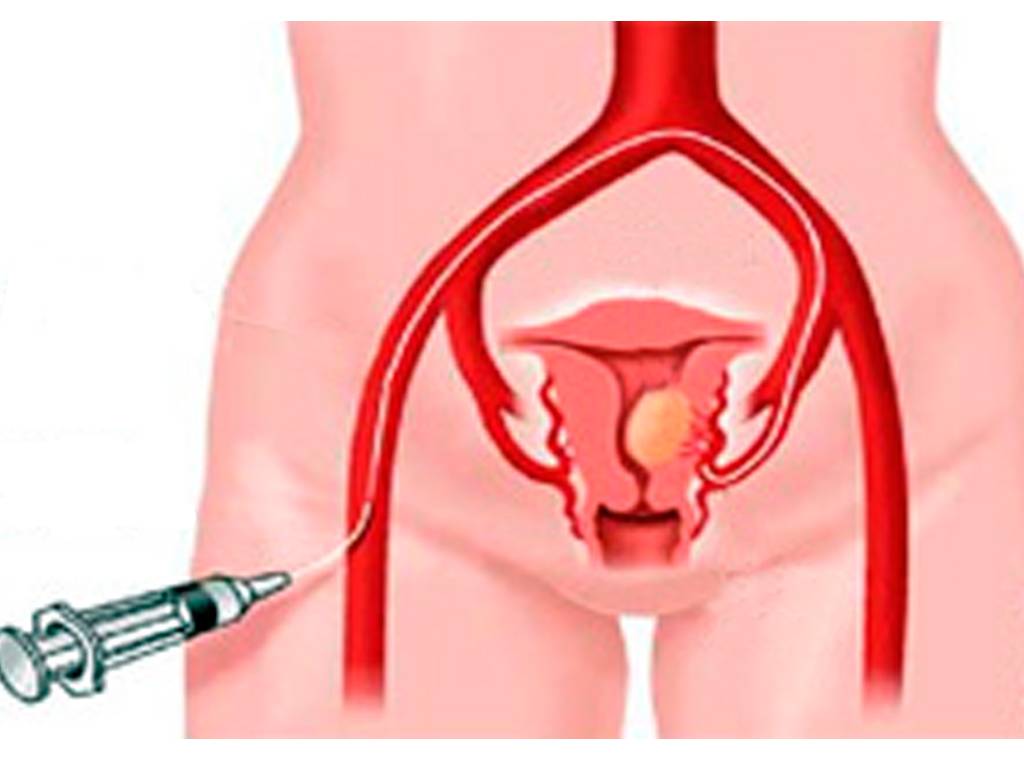
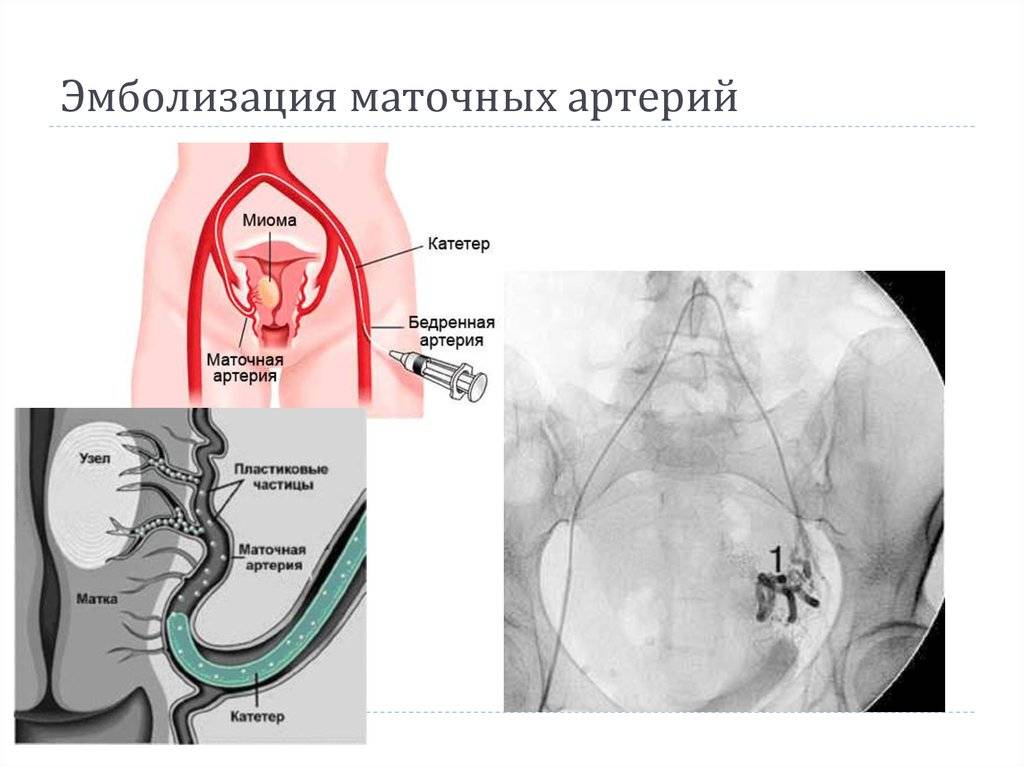
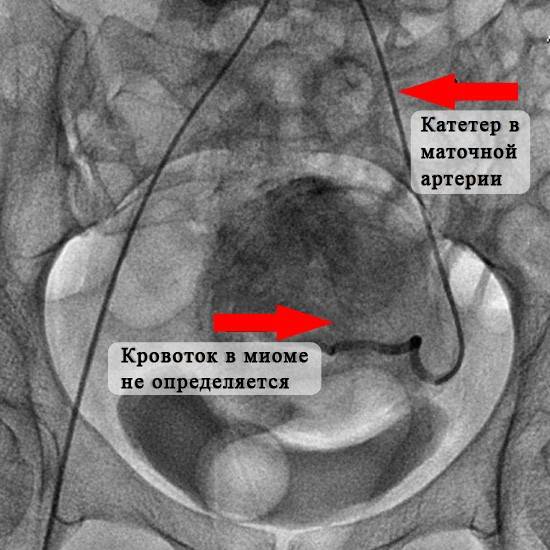
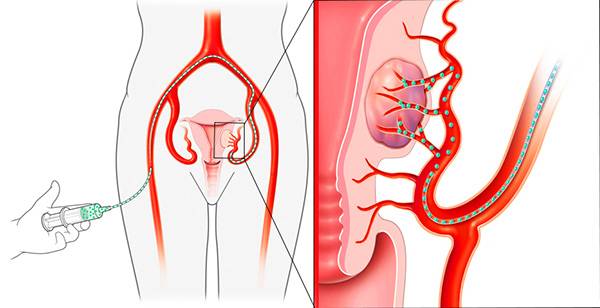
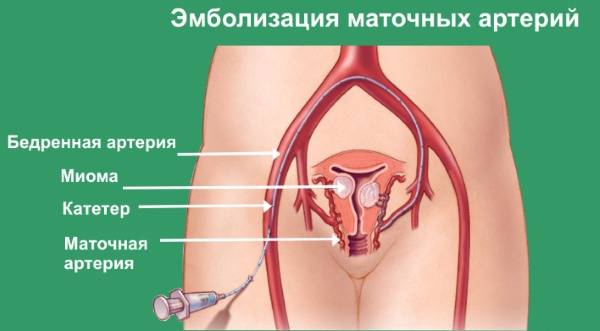
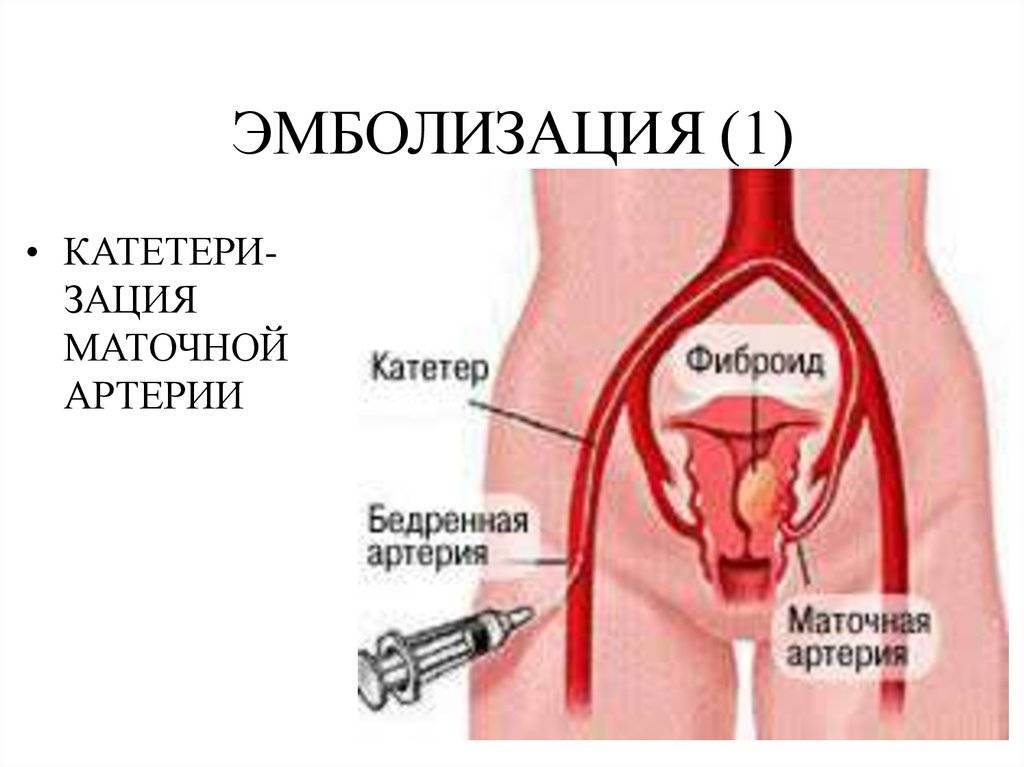
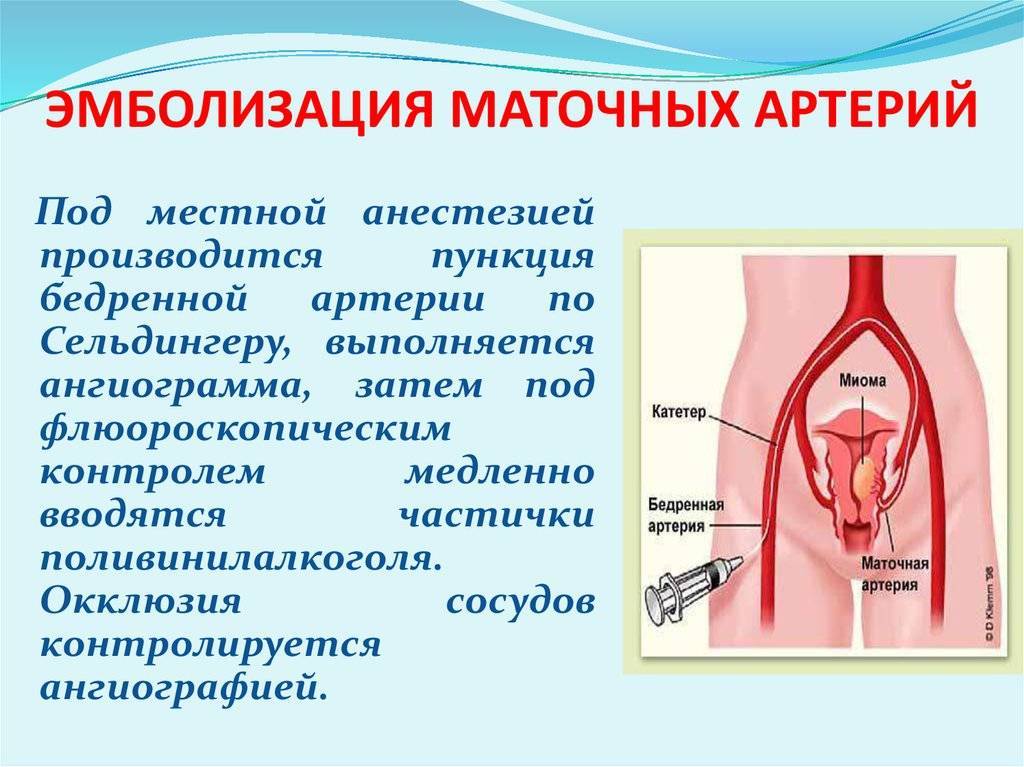
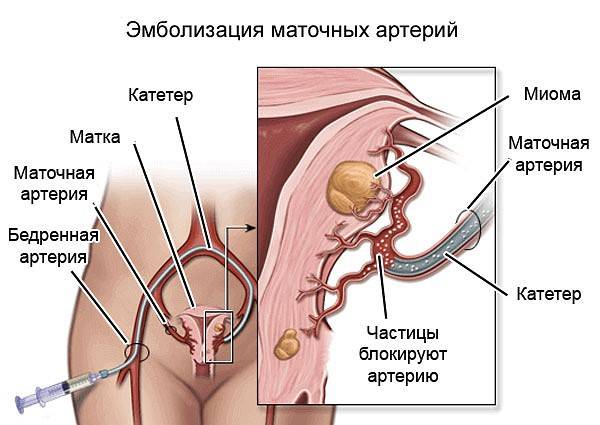
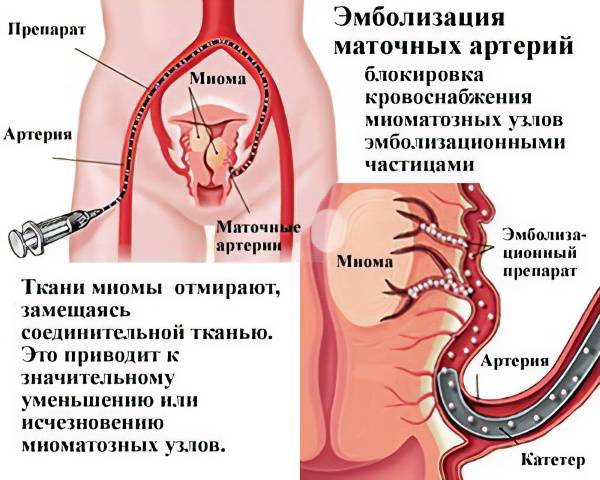
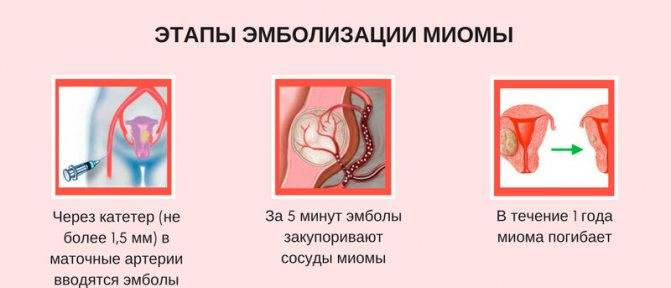
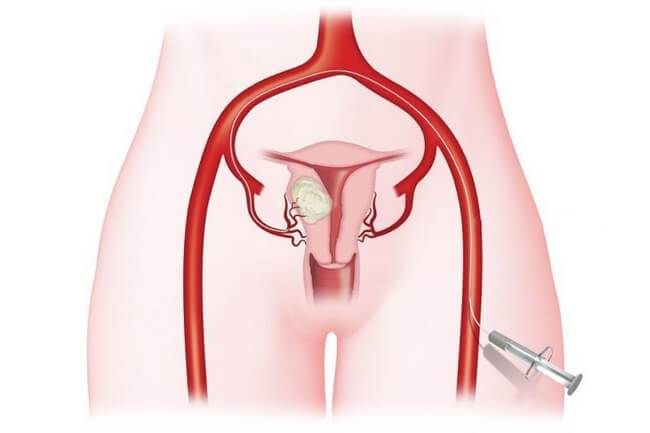
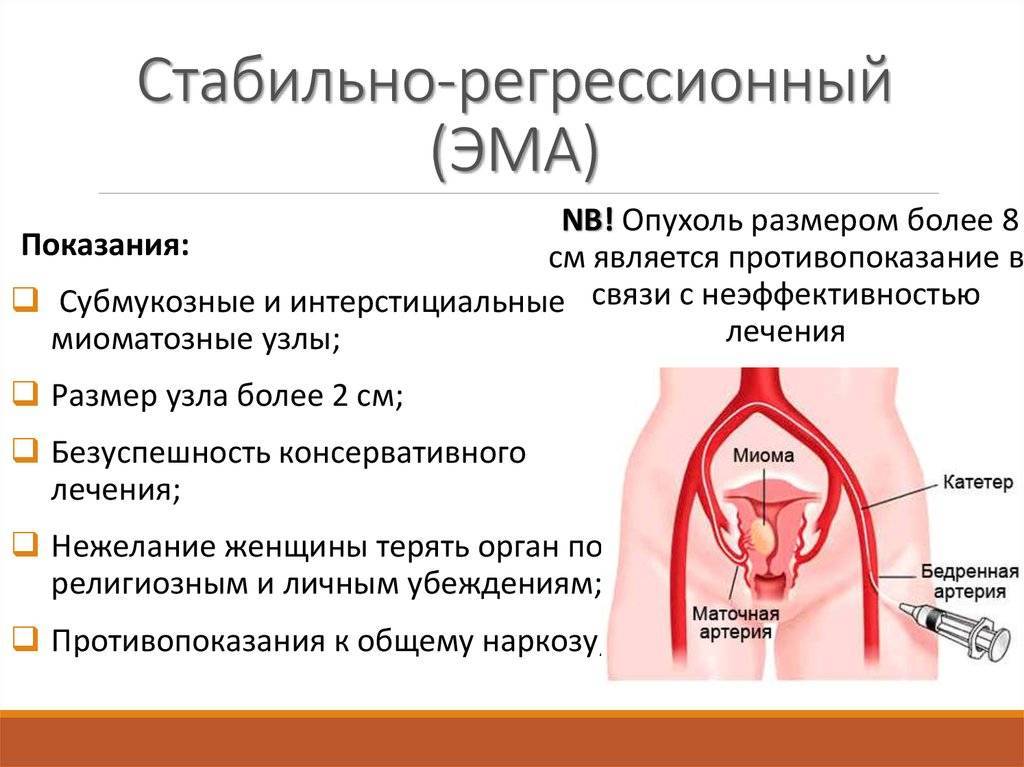
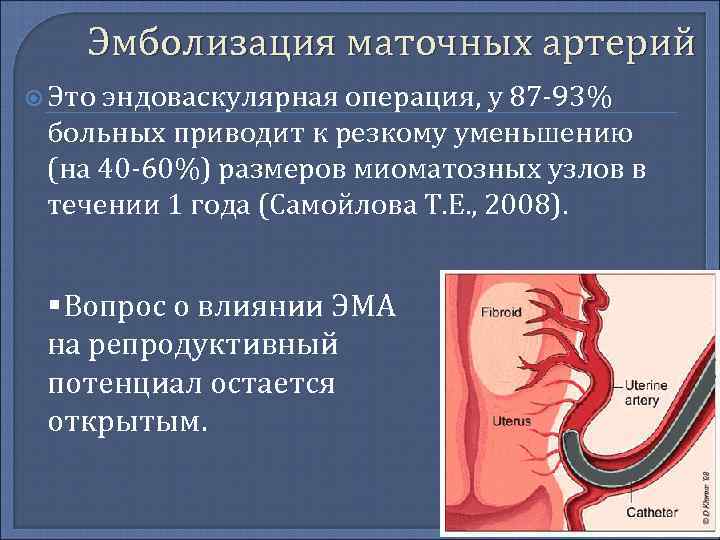
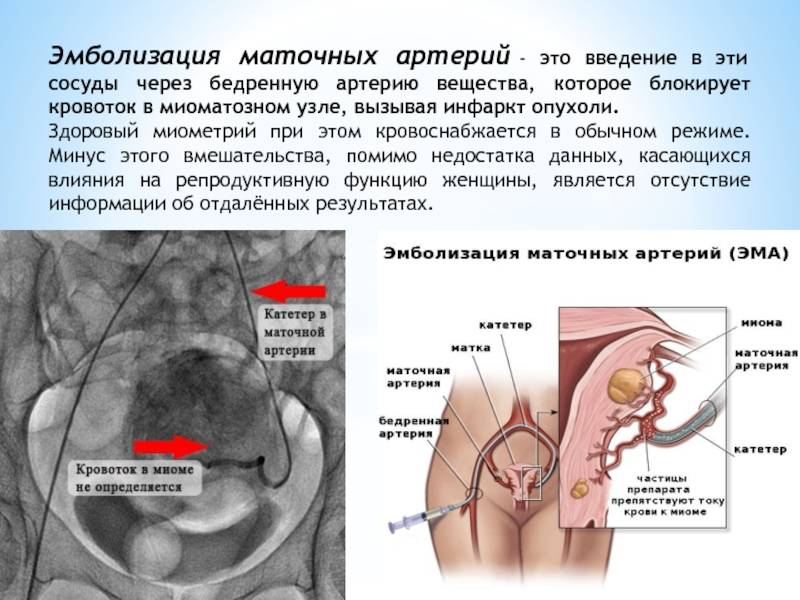
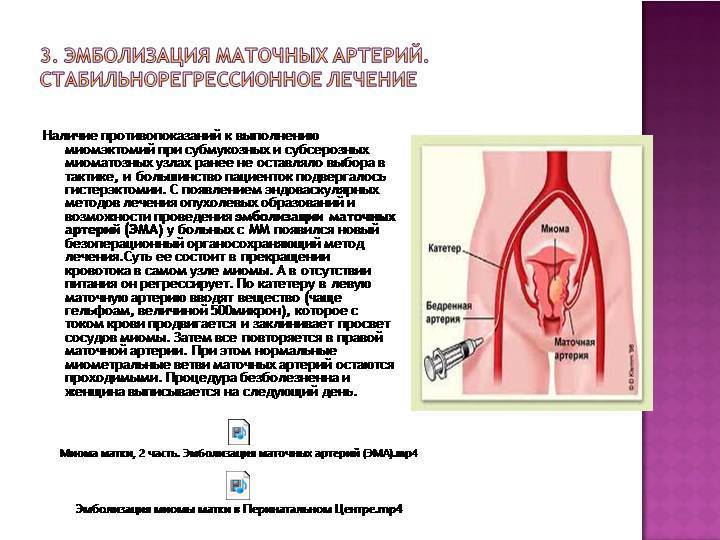
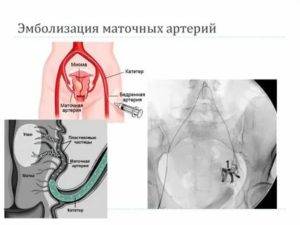
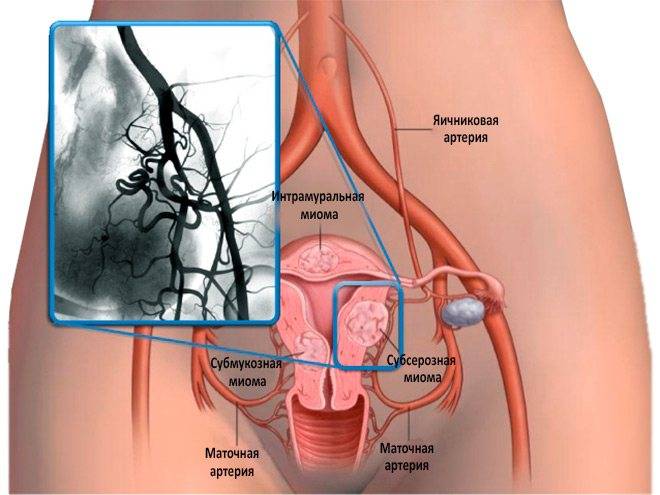
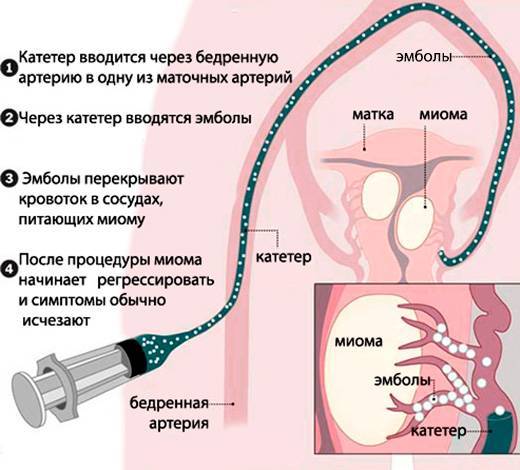
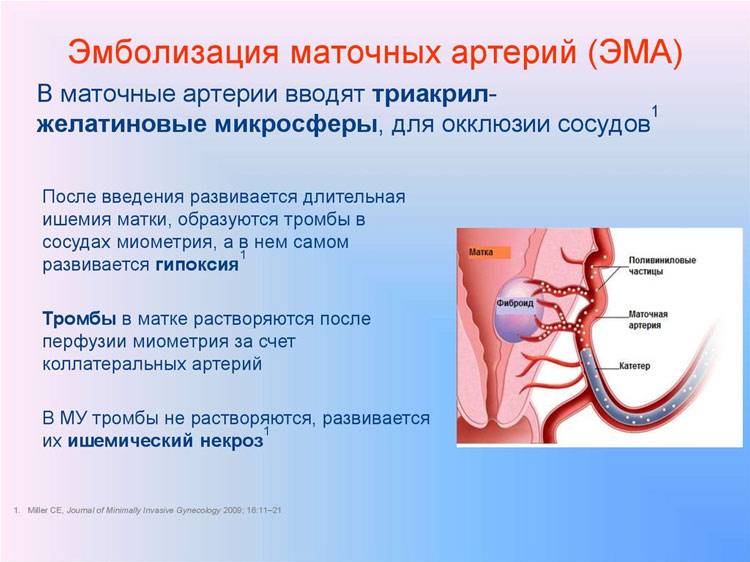
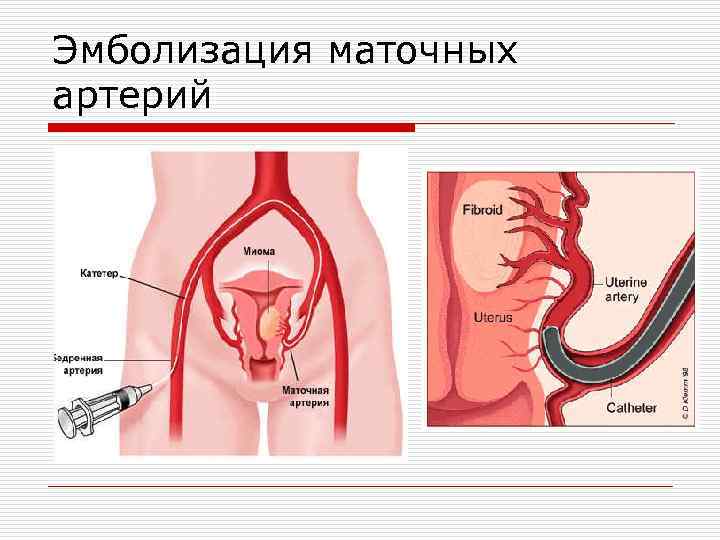
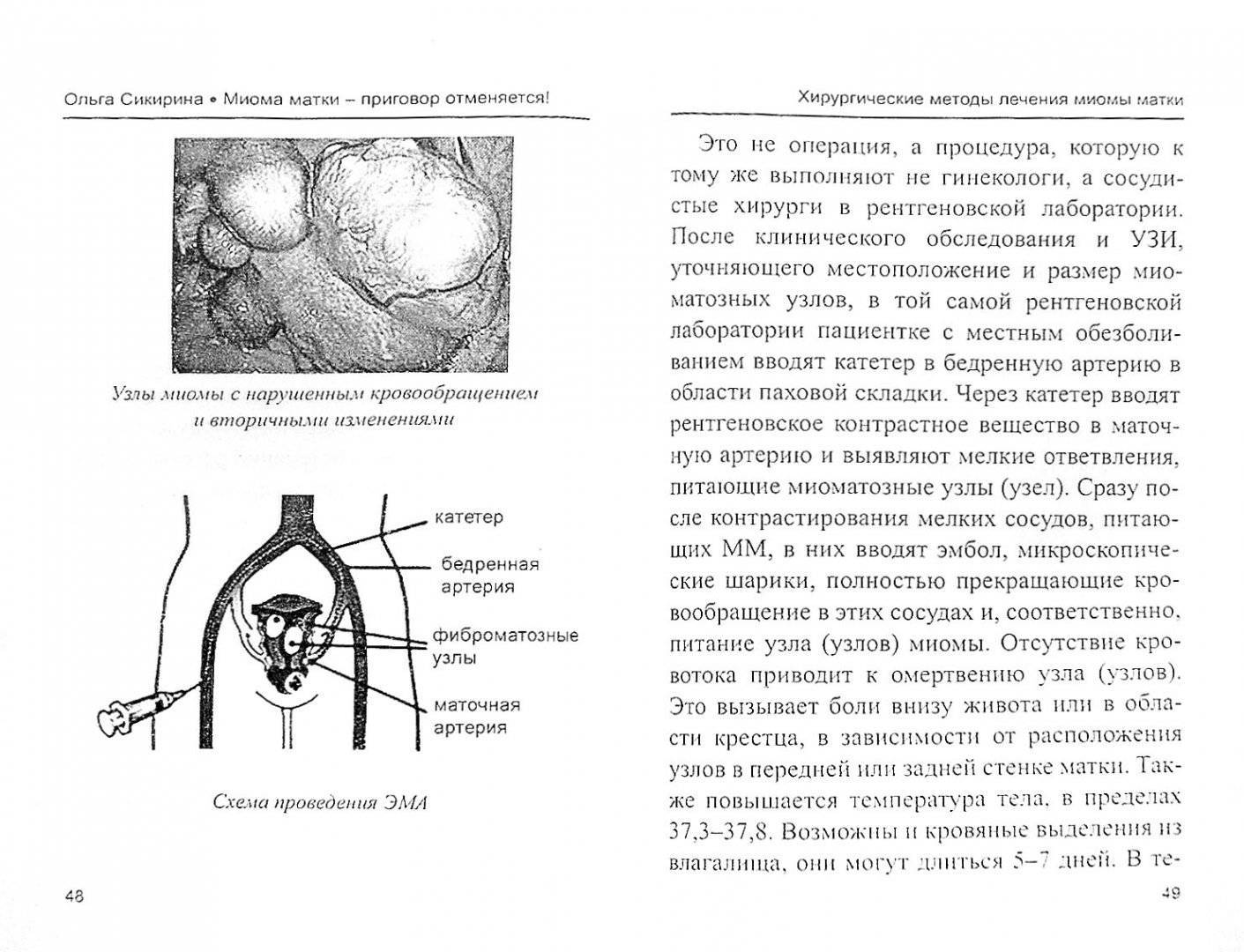
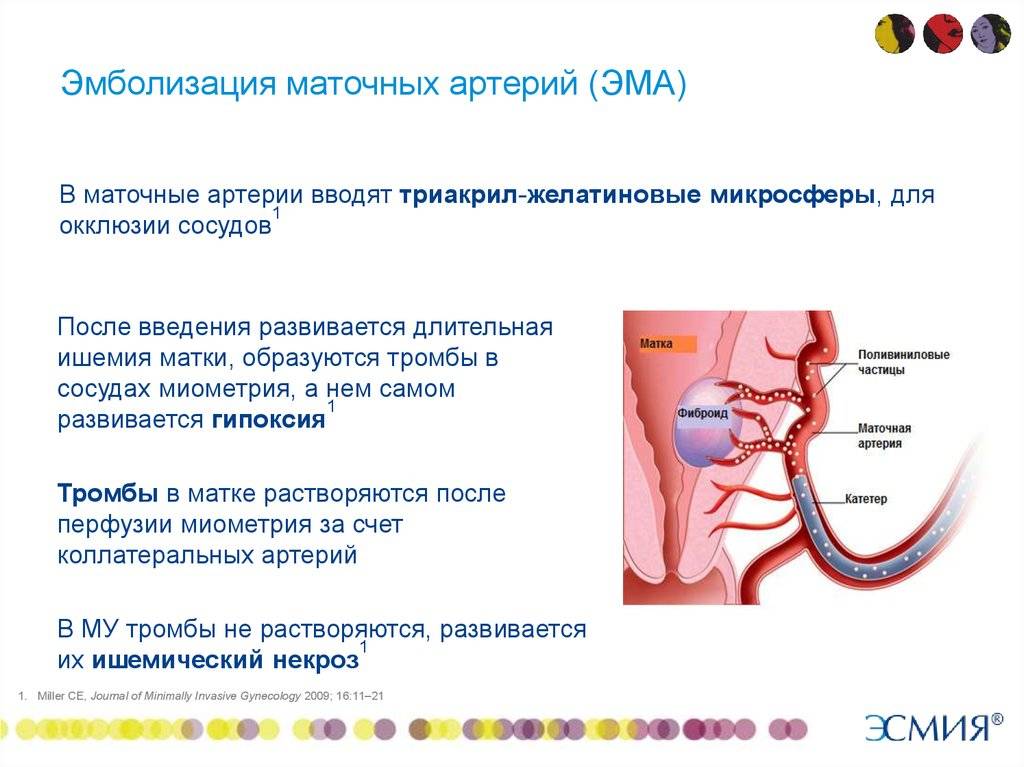
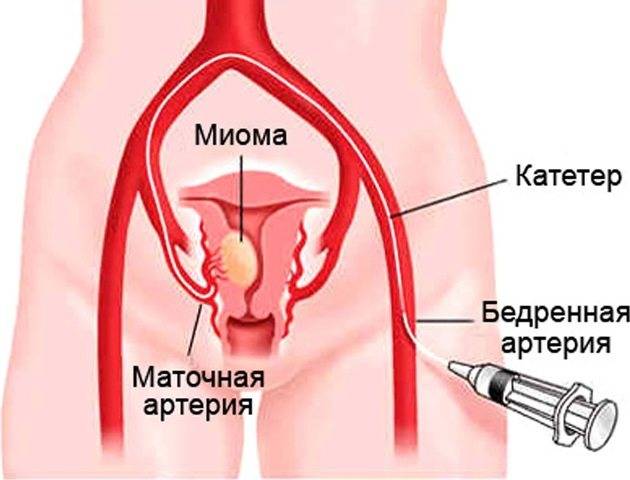
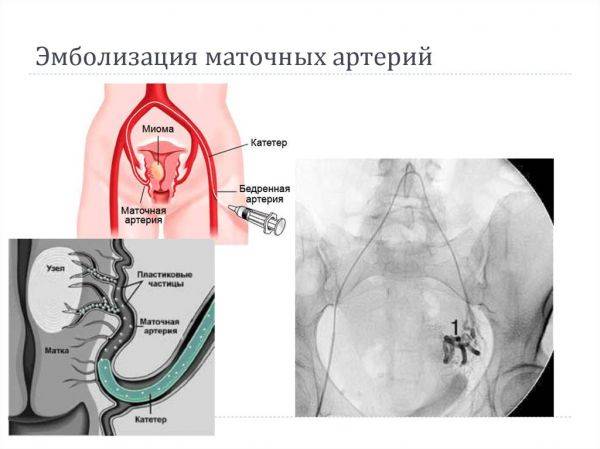
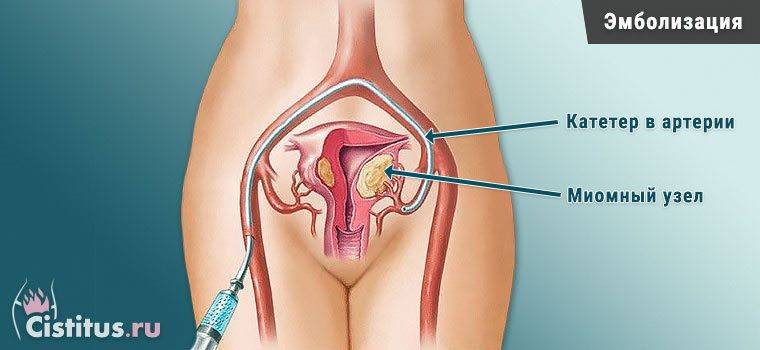
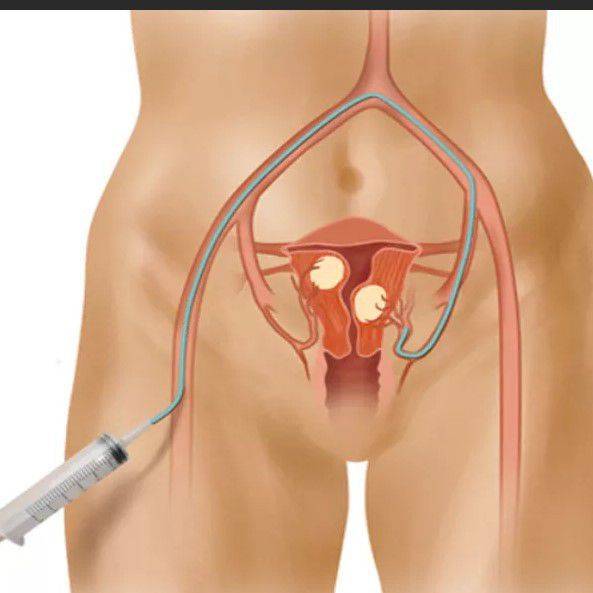
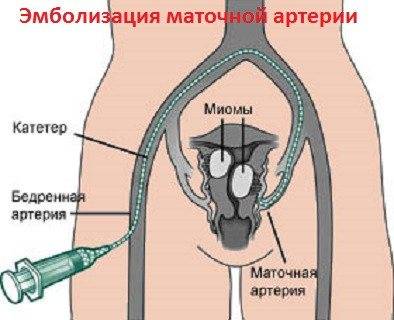
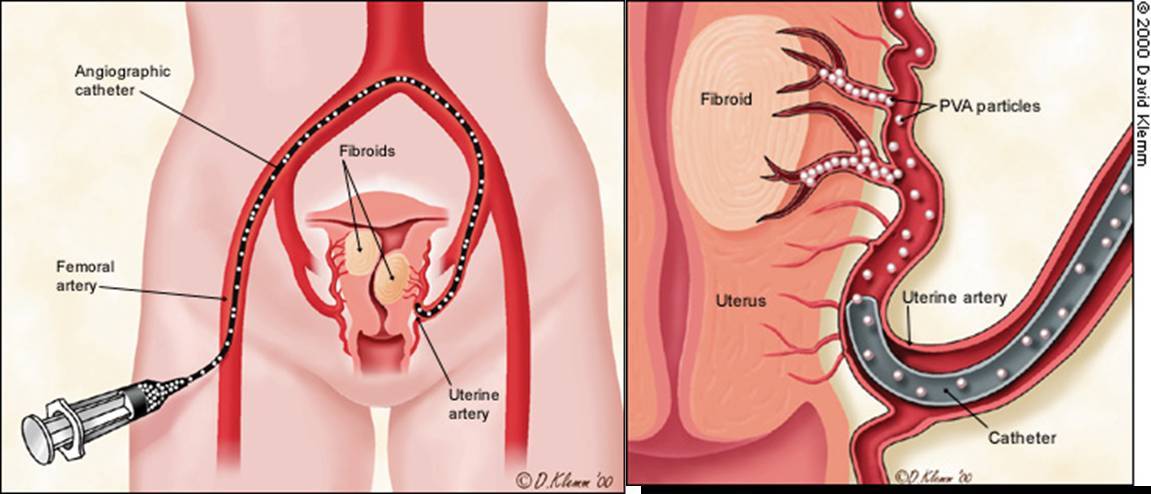
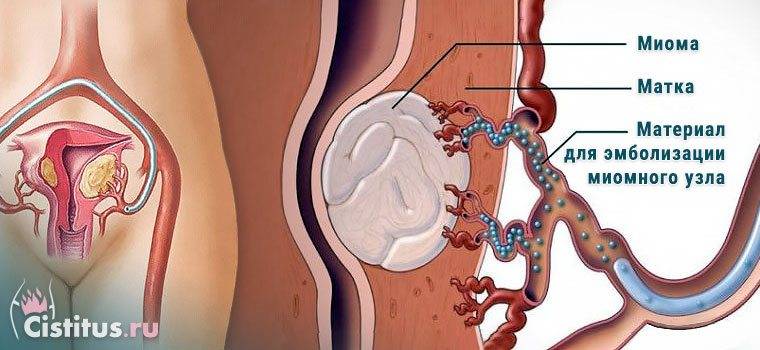
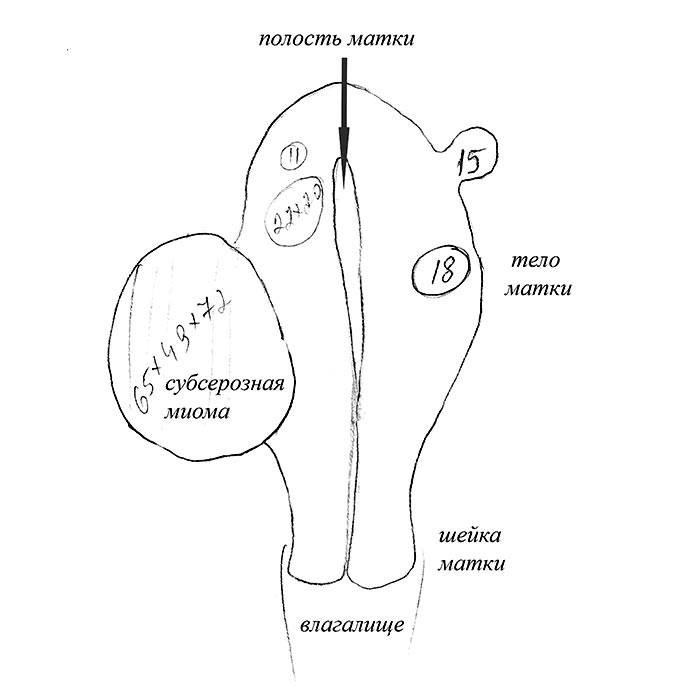
Отделение миоматозного узла в брюшную полость
Это еще одно мифологическое осложнение. Речь идет о миоматозных узлах «на ноже», которые растут снаружи матки на тонком основании. Еще такие узлы называют субсерозными на тонком основании. Дело в том, что часть врачей исходят только из своих рассуждений, предполагая, что если проводить эмболизацию маточных артерий при наличии таких узлов, ножка этого узла некротизируется и узел «отделится» от матки и упадет в брюшную полость, что потребует срочного хирургического лечения. На самом деле за всю историю проведения ЭМА ни одного такого случая не было описано. Более того, в 2006 году было проведено отдельное исследование: группе пациенток именно с такими узлами проводилась ЭМА и оценивались отдаленные результаты. В итоге было показано, что узлы от матки не отделяются и никаких особенностей в результатах ЭМА и состоянии пациенток после процедуры нет. Таким образом, данное осложнение — миф.
Абстракт:
J Vasc Interv Radiol. 2009 Sep;20(9):1172-5. Epub 2009 Jul 29.
Safety and effectiveness of uterine artery embolization in patients with pedunculated fibroids.
Smeets AJ, Nijenhuis RJ, Boekkooi PF, Vervest HA, van Rooij WJ, de Vries J, Lohle PN.
Source
Department of Radiology, St. Elisabeth Ziekenhuis, Hilvarenbeekseweg 60, 5022 GC Tilburg, The Netherlands. radiol@eztilburg.nl
Abstract
PURPOSE:
To assess complications and outcomes of uterine artery embolization (UAE) in women with pedunculated fibroids in a large single-center patient cohort.
MATERIALS AND METHODS:
From a database with prospectively collected data from 716 women treated with UAE between 1996 and 2008, 29 women were identified with 31 pedunculated fibroids. Magnetic resonance images obtained before and 3 months after UAE were used to calculate stalk diameter change and volume reduction of both the pedunculated fibroid and uterus. Two observers assessed the overall percentage infarction and infarction of pedunculated fibroid. Complications were recorded and long-term clinical follow-up (mean, 33 months; range, 10-78 months) assessed with use of a questionnaire.
RESULTS:
The mean reduction in uterine and pedunculated fibroid volume was 37% and 33%, respectively. The mean reduction in stalk diameter was 0.3 cm (95% confidence interval : 0.18, 0.52 cm) or 13% from initial mean diameter. Stalk enhancement was not affected by UAE. The mean pedunculated fibroid infarction and mean overall infarction rates were 87% and 92%, respectively, for observer 1 and 88% and 92% for observer 2, with good interobserver variability. All women returned the questionnaire and no early or late complications of UAE were reported (0%; 95% CI: 0.0%-13.9%).
CONCLUSIONS:
In this small series of pedunculated subserosal fibroids treated with UAE, no complications occurred. The findings suggest that the use of UAE to treat pedunculated subserosal fibroids may be safe and effective. PMID: 19640736
Подготовка и проведение
Удаление миомы матки методикой лапароскопии может быть консервативным и радикальным. Консервативное вмешательство подразумевает использование миомэктомии лапароскопическим способом. Данная методика относится к щадящим операциям. Лапароскопическая миомэктомия означает удаление миомы матки с сохранением здоровых тканей.
Лапароскопическая миомэктомия рекомендована женщинам репродуктивного возраста и является предпочтительным методом удаления. После миомэктомии женщина сохраняет репродуктивную функцию.
Лапароскопия миомы матки радикальным способом или гистерэктомия означает ампутацию тела матки. Такая лапароскопическая операция зачастую проводится пациенткам при больших размерах новообразований и после наступления менопаузы.
Послеоперационный период при радикальной лапароскопии отличается от миомэктомии более тяжёлой реабилитацией.
Перед проведением лапароскопической операции, например, миомэктомии, необходимо провести детальное обследование пациентки. Это позволит уточнить размер, локализацию и вид образований. При больших размерах опухоли лапароскопическая методика может быть противопоказана.
Предоперационная подготовка к лапароскопии включает:
- фиброгастродуоденоскопию;
- ЭКГ;
- коагулограмму;
- общее клиническое исследование крови;
- биохимия;
- общий анализ мочи;
- ПЦР на половые инфекции;
- соскоб на онкоцитологию;
- диагностическое выскабливание матки и гистероскопию;
- исследование на наличие ВИЧ, вирусных гепатитов и сифилиса.
Лапароскопия выполняется в несколько последовательных этапов.
- Проведение эпидуральной анестезии или общего обезболивания.
- Выполнение четырёх проколов небольших размеров в брюшине, что необходимо для помещения инструментов.
- Заполнение брюшной полости углекислым газом для возможности осуществления операции.
- Введение лапароскопа.
- Удаление новообразований, а также маточного тела при необходимости.
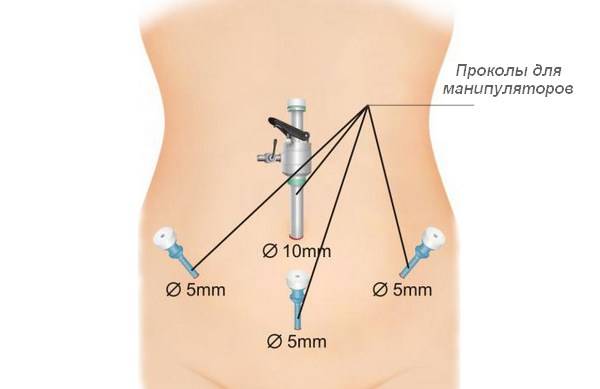
По продолжительности лапароскопия занимает около двух часов. Вскоре после операции женщине разрешается вставать и ходить.
Общая диагностика перед проведением эмболизации маточных артерий включает:
- гинекологическое УЗИ;
- общие анализы крови и мочи;
- коагулограмма;
- мазок на флору;
- цитологическое исследование;
- ПЦР на половые инфекции;
- обследование на ВИЧ и некоторые виды гепатита;
- кольпоскопию;
- ЭКГ.
Перед госпитализацией женщине необходимо получить заключение о состоянии здоровья у терапевта. Накануне проведения вмешательства не рекомендуют принимать пищу. В некоторых случаях пациентке следует носить компрессионное бельё за несколько дней до ЭМА и во время процедуры. За час до процедуры возможно введение успокоительного препарата.
ЭМА проводят в операционной, оснащённой ангиографическим аппаратом
Непосредственно перед началом манипуляции эндоваскулярный хирург уточняет у пациентки, нет ли у неё аллергической реакции, что важно при использовании эмболизирующих веществ
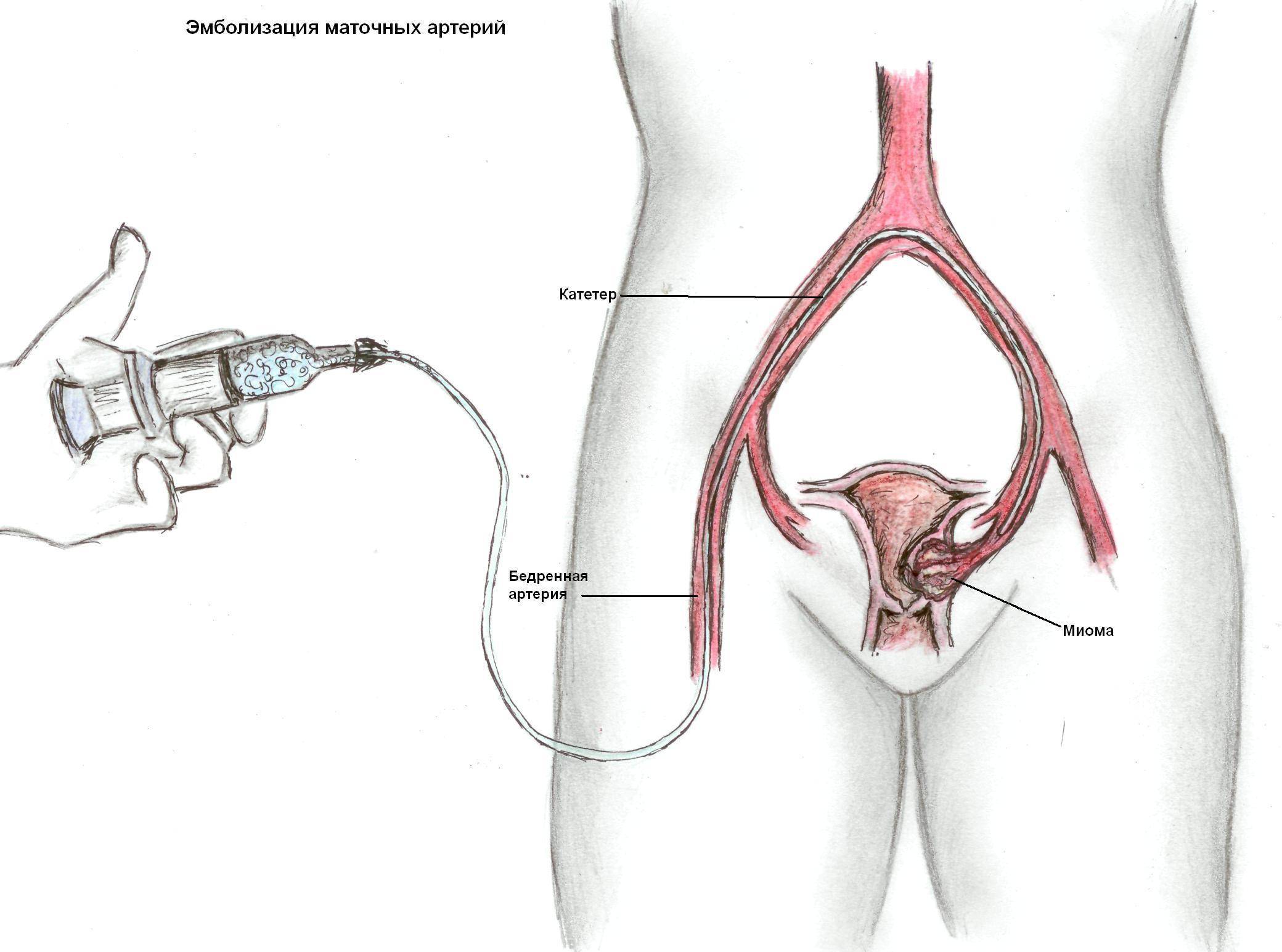
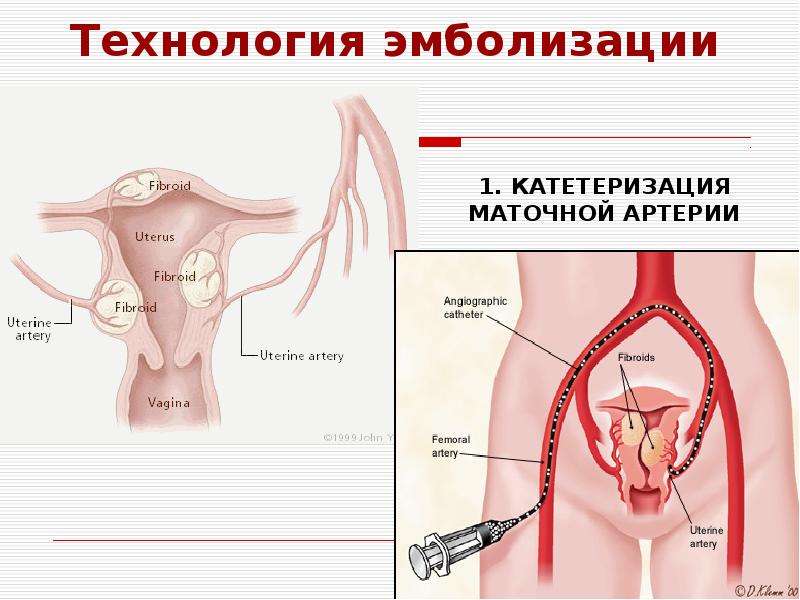
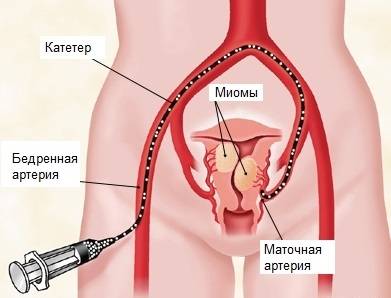
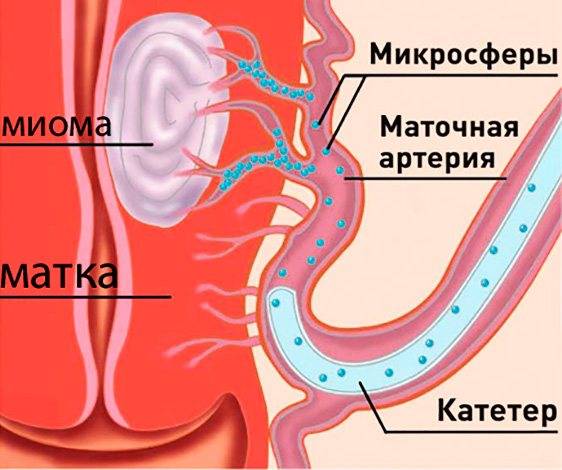
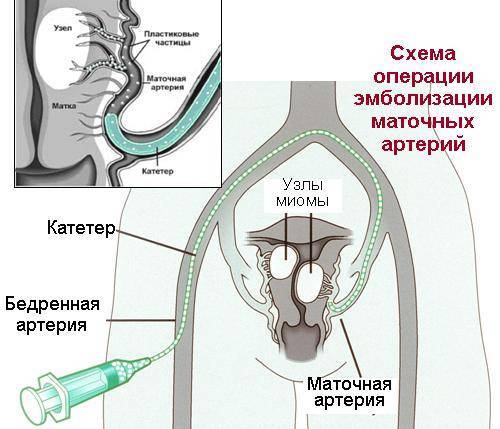
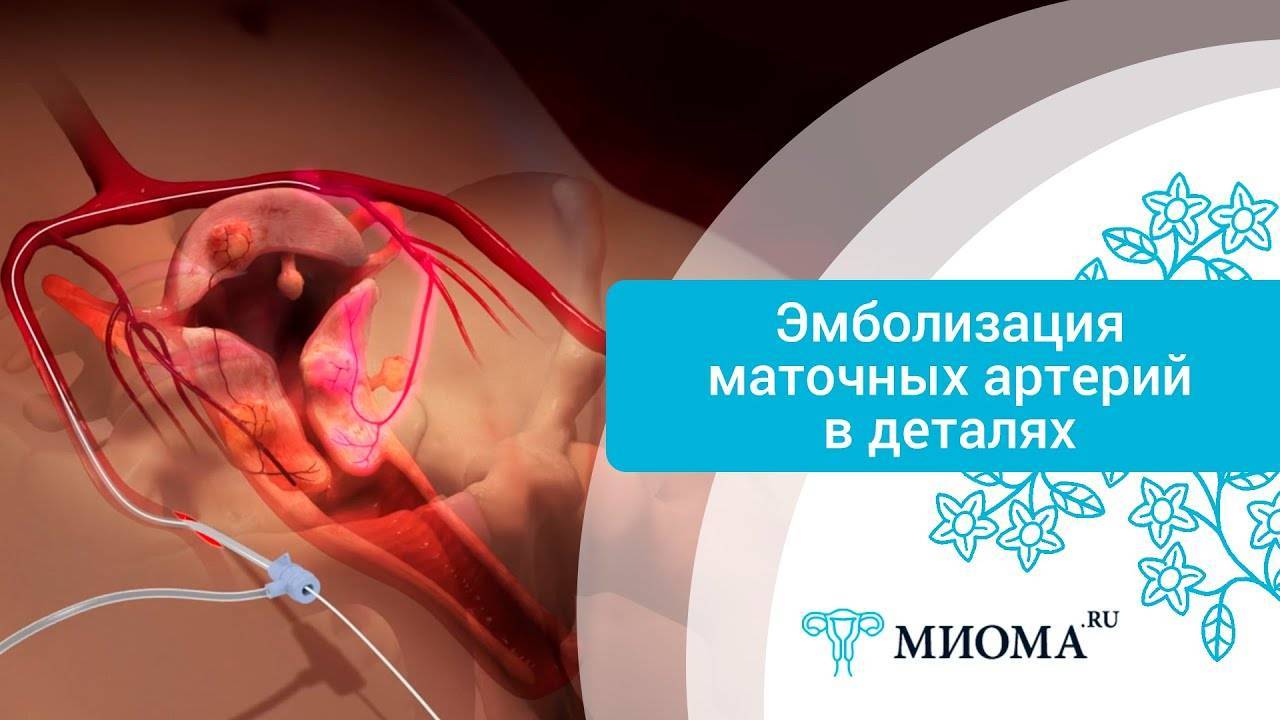
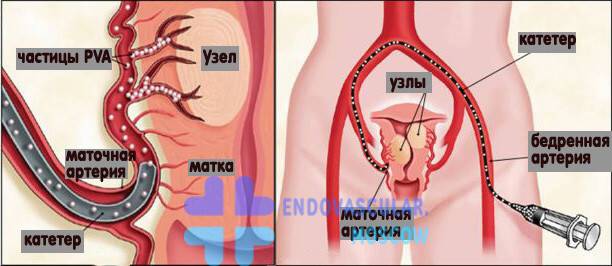
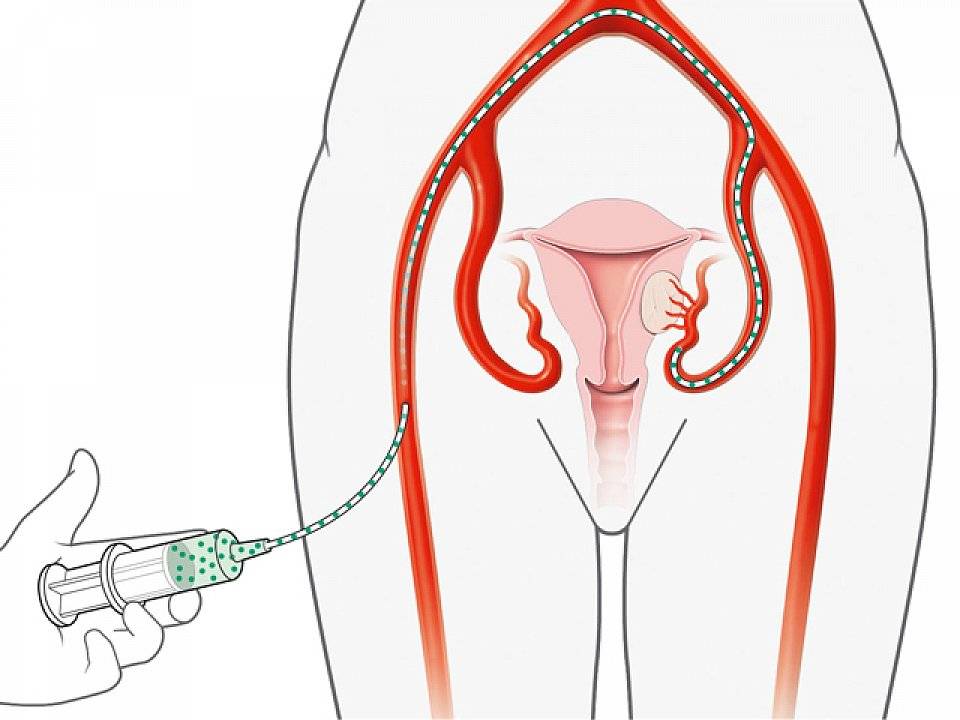
Пациентка находится на ангиографическом столе. Перед эмболизацией маточных артерий проводится анестезия и обработка живота и правого бедра антисептиком. При помощи прокола в бедренную артерию помещают небольшой катетер, а затем проводят эмболизирующие частицы.
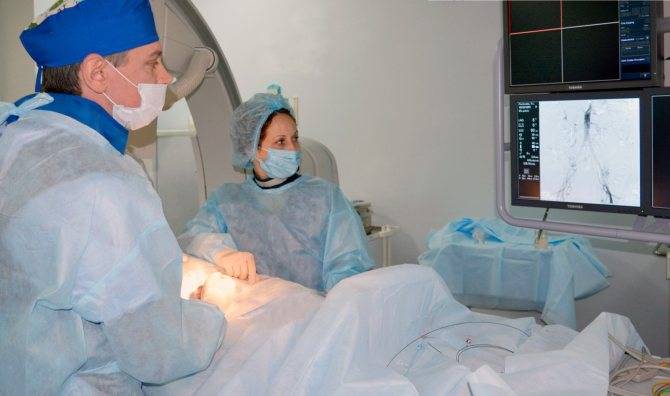
Эмболизация маточных артерий занимает не более трёх часов. Во время процедуры может возникать незначительное жжение. После проведённой эмболизации маточных артерий катетер удаляется, а на область бедра врач накладывает повязку. В некоторых случаях перед выполнением эмболизации маточных артерий следует провести диагностическое выскабливание.
Эмболизация артерий в онкологии
Эмболизация сосудов при некоторых видах рака также имеет высокую эффективность. Начальные стадии диагностированной карциномы поддаются лечению путем купирования кровотока. Специалисты успешно лечат введением радиоизтопов начальные стадии рака почек, легких, органов малого таза, мочевого пузыря, кишечника, простаты, новообразований в головном мозге и т. д.
Суть применения эмболизации для онкопациентов сводится в препятствовании питания пораженной ткани, насыщенной кислородом и питательными веществами крови. Атипические клетки без подпитки прекращают свой рост и погибают. Успешность лечения зависит от стадии заболевания и ее локации.
В более серьезных случаях запущенного рака и опухолей злокачественного характера больших размеров эмболизацию применяют для уменьшения новообразования. Процедура показана:
- при кровотечениях, вызванных раком;
- в случае интенсивного роста опухоли;
- для купирования болевого синдрома, когда новообразование давит на органы, расположенные рядом;
- сокращение образования метастаз.
Метод эмболизации классифицируют на самостоятельный (для начальных стадий рака), предоперационный (для уменьшения размеров опухоли) и паллиативный (для облегчения страданий больного онкологией).
Эмболизация и рентгеновское облучение
Доза рентгеновского излучения — это больше миф, чем реальное осложнение. Во время эмболизации маточных артерий используется особый вид рентгеновского излучения — оно более мягкое по сравнению с тем, которое рутинно используется для обычных снимков. К примеру, когда вам делают снимок грудной клетки, по интенсивности излучения это можно сравнить с мощным светом, который направлен на вас из прожектора. Это необходимо, чтобы четко разглядеть все ткани и кости. А теперь представьте, что тот же прожектор светит на вас, но уже через ставни — свет проходит в комнату, но он рассеянный и неяркий. Именно такое — мягкое и рассеянное — излучение используется во время ЭМА. Это позволяет видеть только необходимое для проведения процедуры: сосуды, катетеры, контрастное вещество.
Суммарное время излучения во время процедуры редко превышает 2–3 минуты (конечно, если процедуру проводит опытный врач). Получается, что 2–3 минуты такого рассеянного излучения соответствует, по сути, одному рентгеновскому снимку грудной клетки.
Тут можно возразить, что излучение направлено на область яичников, и это может быть опасно. На самом деле это не так. В гинекологии уже много десятков лет используется метод проверки проходимости маточных труб, который назначается пациенткам, страдающим бесплодием. Во время этой процедуры в полость матки вводится контрастное вещество, выполняется два полноценных рентгеновских снимка области придатков, чтобы оценить прохождение этого вещества по трубам и попадание его в брюшную полость. Лучевая нагрузка этих двух снимков в среднем соответствуют той, что применяется во время проведения ЭМА. Напомним, что такие снимки делают женщинам, которые планируют беременность. Таким образом, доза рентгеновского облучения во время эмболизации минимальна и совершенно безопасна.
Почему некоторые гинекологи высказываются против ЭМА?
На самом деле все было бы нормально и нам бы не пришлось писать эту статью, если бы эмболизацию маточных артерий выполняли сами гинекологи. Именно эта простая причина лежит в отрицании этого метода.
Миома матки является основной хирургической патологией в гинекологии. Другими словами, наибольшее количество операций (до 80% от общего числа), которые выполняются гинекологами, выполняется по поводу миомы матки. Чаще всего это ампутация матки и несколько реже — удаление узлов миомы. При этом эмболизация маточных артерий является достойной альтернативой хирургическому вмешательству в 60–70% всех случаев миомы, а это приведет к существенному оттоку пациентов из гинекологических стационаров, снижению там количества операций и, разумеется, к снижению персональных доходов гинекологов.
Еще один важный фактор: для проведения эмболизации маточных артерий необходимо специальное (весьма дорогостоящее) оборудование и наличие опытного эндоваскулярного хирурга — условия, которые реализованы не более чем в десяти-пятнадцати клиниках по всей России. При этом гинекологических стационаров и отделений в нашей стране тысячи. Таким образом, организовать проведение эмболизации маточных артерий во всех гинекологических клиниках при всем желании невозможно (и, как показывает опыт развитых стран, совершенно не нужно). Значит, если гинекологи будут объективно предоставлять информацию об эмболизации маточных артерий и направлять пациентов на ЭМА в крупные специализированные клиники — они фактически будут терять большую часть пациентов, которым можно оказать хирургическую помощь в их стационаре, улучшить показатели работы стационара, а также свое материальное положение, чего уж скрывать. Классический конфликт интересов!
Вот такая получается сложная ситуация, и она характерна не только для нашей страны. Похожая проблема есть во многих странах, где выполняется ЭМА. Есть чисто хирургические центры, которые внушают пациентам настороженное отношение к этой операции, направляя на ЭМА только тех, у кого совершенно неоперабельная с хирургической точки зрения ситуация, а есть крупные клиники, где имеются все методы лечения миомы матки (от хирургии до ЭМА). Очевидно, что в таких клиниках есть возможность объективно оценивать ситуацию и беспристрастно рекомендовать лечение. Выбор метода лечения у конкретного пациента не должен быть ограничен недостатком технических, профессиональных либо организационных возможностей клиники.
Однако в развитых странах этот период «безапелляционного отрицания» уже пройден — благодаря наличию серьезных юридических механизмов, не позволяющих скрывать информацию обо всех лечебных возможностях.
Еще раз повторим: если бы ЭМА проводилась силами гинекологов — никаких проблем бы не было. Именно это произошло с лапароскопией — период критичного отношения к этому способу проведения операции (пришедшему в гинекологию из абдоминальной хирургии) длился недолго, хотя и сопровождался очень резкими нападками на врачей, начавших ее использование. Теперь лапароскопия доступна практически во всех клиниках и доля полостных операций свелась к минимуму; но лапароскопию проводят гинекологи, поэтому пациенты никуда не делись. Если бы лапароскопия осталась бы прерогативой только абдоминальных хирургов и гинекологи не могли бы ее проводить — увы, тогда бы отношение многих гинекологов к этому методу было бы таким же, как и к ЭМА.

Однако в настоящее время в развитых странах именно отношение к ЭМА стало той «лакмусовой бумажкой», позволяющей пациентам определить уровень профессиональной компетенции своего гинеколога. В частности, это было продемонстрировано в статистическом исследовании, опубликованном американским журналом Medical Devices & Surgical Technology Week, результатом которого стали следующие выводы:
-
- Около 76% гинекологов первоначально высказывались против ЭМА, однако 43% изменили свое отношение к ЭМА после того, как их пациентки выполняли это вмешательство.
- В 90% случаях пациентки сами начинали обсуждать вопрос об ЭМА со своим гинекологом, и лишь в 5% случаев это была инициатива гинеколога.
В России ситуация существенно хуже. Как видите, тенденция одна: про ЭМА пациенты узнают сами из Интернета, сами рассказывают об этом методе лечения своим врачам и довольно часто меняют врача, если он изначально был против. И совершенно очевидно, что ЭМА этим пациентам помогла и они уже не могут доверять врачу, который был против этого метода лечения.
Показания: кому рекомендована операция
Миома матки – это доброкачественная опухоль миометрия (мышечного слоя детородного органа). По данным аутопсии (посмертного вскрытия) патология выявляется у 80% всех женщин. Клинически заболевание проявляется только у 35% представительниц прекрасного пола. Обычно миома дает знать о себе после 40 лет, но возможно появление опухоли и в более молодом возрасте. Довольно часто патология впервые выявляется при беременности или на этапе планирования ребенка.
Для лечения миомы матки применяются разные методы, но ЭМА среди них занимает особое место. Манипуляция эта не нова: первые попытки делать эмболизацию ветвей маточных артерий проводились еще в 1979 году, однако широкого распространения процедура не получила. Только в 90-х годах прошлого века ЭМА стала применяться для лечения миомы. Сегодня прогрессивные клиники предлагают эмболизацию как самый эффективный и вместе с тем безопасный вариант решения проблемы.
Теоретически данная операция может проводиться всем пациенткам, однако на практике все не так просто. Есть определенные показания, при которых ЭМА принесет желаемый результат:
- Единичные и множественные миоматозные узлы любого размера с хорошим кровоснабжением (кроме интрамурально-субсерозных опухолей);
- Интрамурально-субсерозные миомы размерами до 8 см;
- Крупные и/или субсерозные узлы при множественной миоме – в качестве одного из этапов лечения (подготовка к консервативной миомэктомии);
- Маточное кровотечение при миоме, когда другие методы не эффективны;
- Миома у женщины, планирующей беременность.
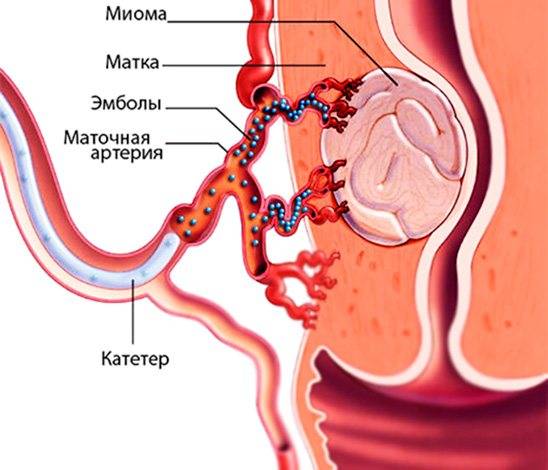
В норме маточные артерии маленькие по диаметру и введение в них катетера невозможно, но при возникновении миомы их диаметр увеличивается в соответствии с размерами опухоли.
Лечение миомы методом ЭМА однозначно показано при наличии множественных узлов. Обычную миомэктомию при таком диагнозе выполнить довольно сложно: слишком высок риск повреждения здоровой ткани. До внедрения ЭМА единственным способом лечения было удаление матки. Сегодня врач может прекратить кровоснабжение опухолевых узлов и тем самым решить проблему с минимальным риском для пациентки.
Подготовка женщины к эмболизации

Прежде чем пройти процедуру ЭМА, пациентка должна обследоваться.
- Клиническое обследование проводит врач гинеколог: уточняется анамнез, осуществляется общий осмотр, осматриваются молочные железы, пальпируются органы брюшной полости, измеряются пульс и артериальное давление на обеих руках.
- Гинеколог выполняет гинекологическое обследование: влагалище и шейка матки осматриваются в зеркалах, осуществляется бактериоскопическое (забор материала из цервикального канала, влагалища, уретры) и цитологическое (забор материала из эндо- и экзоцервикса) исследования, бимануальное влагалищное исследование.
- Необходим ряд лабораторных обследований: общие анализы крови и мочи, биохимическое исследование крови, коагулограмма, определение группы крови и Rh-фактора, исследование крови на ВИЧ и сифилис, забор крови на онкомаркёры.
- Обязательны функционально-инструментальные обследования: ЭКГ, УЗИ органов малого таза и допплерометрия, РДВ (раздельное диагностическое выскабливание) под контролем гистероскопии.
- Показана консультация терапевта и рентгенолога.
Такой метод диагностики, как УЗИ, даёт возможность оценить величину миоматозных узлов, уточнить их количество, обнаружить сочетанную скрытую патологию. Решение вопроса в пользу эмболизации принимается только после оценки данных УЗИ-обследования.
Перед ЭМА пациентке проводится допплерография, которая позволяет дать оценку кровотоку в сосудах, обеспечивающих питанием узлов. Допплерометрия даёт возможность отличить миому от злокачественного образования, что играет решающую роль в выборе методики лечения. Кровоток с высокой скоростью и наличие эхоструктур неоднородного характера в полости матки – признаки, свидетельствующие в пользу саркомы.
РДВ под контролем гистероскопии, которое даёт чёткое представление о клинической картине заболевания, показано в определённых случаях:
- длительное кровотечение маточного генеза, не поддающееся консервативной терапии;
- предполагается наличие процессов патологического характера в эндометрии (например, гиперплазия эндометрия).
За 5 дней до эмболизации прописываются антибактериальные препараты (Орнидазол) для приёма внутрь, что позволяет уменьшить риск вероятных осложнений бактериальной природы. За два часа до начала выполнения ЭМА прописывается ещё антибактериальный препарат (Цефтриаксон). Очистительная клизма осуществляется за сутки до операции. Катетеризация мочевого пузыря проводится непосредственно перед процедурой.
При необходимости назначаются препараты с седативным эффектом. В день осуществления запланированной эмболизации еда и питьё исключаются. Во время манипуляции ноги пациентки должны быть в компрессионных колготках либо чулках, что необходимо для профилактики грозных осложнений тромбоэмболического характера.
Если пациентка принимает препараты, оказывающие действие на свёртываемость крови, лечащий врач должен об этом знать.
ЭМА не осуществляется во время менструации, запланированная операция осуществляется преимущественно в первую фазу цикла.
Плюсы малоинвазивной операции
Терапию миомы матки проводят разными методами, но многие из них неэффективны и нецелесообразны. Гормональная терапия не всегда дает ожидаемый результат, часто заболевание обостряется. Хирургические радикальные способы подразумевают удаление не только опухоли. Нередко, из-за сильного разрастания приходится иссекать весь орган. После такого вмешательства женщина становится бесплодной.
Альтернатива эти методикам есть и она безвредна и безопасна. Это эмболизация миомы в стенках матки — миниинвазивная процедура, заключающаяся в прекращении подпитки (снабжения кровью) узлов. Патологические ткани отмирают. Здоровые зоны органа не травмируются. Метод способствует устранению образования матки, предупреждению рецидива.
По отзывам на эмболизацию маточных артерий (ЭМА) видно, что вмешательство хорошо переносится, почти не имеет осложнений. Процедура не сказывается на работе репродуктивной системы. ЭМА считается способом выбора для девушек с нереализованным материнством.
От иных хирургических методов терапии миомы эмболизация МА отличается:
- Эффективностью. Обострения возникают редко, менее чем в 1% случаев.
- Быстрым устранением неприятной симптоматики. Ощутимое уменьшение узлов происходит на протяжении первых 3-ех месяцев.
- Безопасностью. Вероятность осложнений после эмболизации миомы в теле матки низкая.
- Прицельным воздействием (только на образования). Здоровая ткань сохраняется.
- Малой травматичностью. Выполняется без разреза. Восстановление девушки, которой провели ЭМА, происходит быстро.
- Отсутствие влияния на репродуктивную функцию.
Есть у методики и минусы. Выделяют высокую цену, необходимость проведения рентгенографии, что связано с получением дозы облучения (она небольшая, сравнима с полученной при выполнении флюорографии). Еще один недостаток — отсутствие возможности провести биопсию (чтобы распознать малигнизацию).
Восстановление после эмболизации маточных артерий
Процедура эмболизации позволяет пациентке сравнительно быстро вернуться к привычной жизни. Первые несколько часов (чаще до утра следующего дня) после эмболизации маточных артерий необходимо соблюдать постельный режим и держать забинтованное бедро в горизонтальном положении. На место пункции артерии в первые два часа прикладывают лед, чтобы уменьшить отек и избежать воспаления. Возможно, что медсестра по указанию врача подключит капельницу.
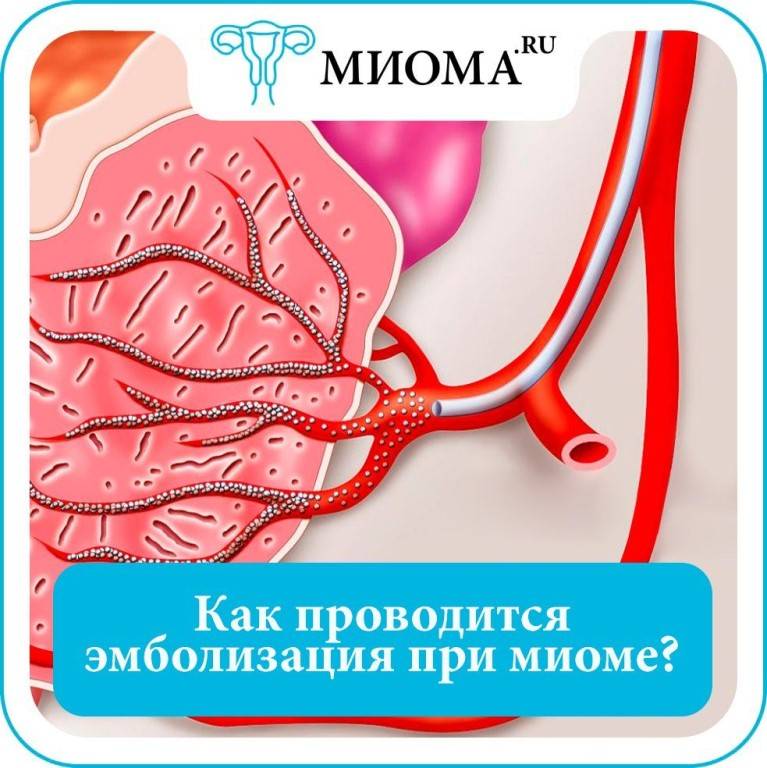
После того, как в маточных артериях прекращается кровоток, клетки миомы начинают испытывать кислородное голодание (ишемия), то есть фактически в них развивается инфаркт. Постепенно в миоме развивается тотальная гибель (некроз) мышечных структур. Следствием всех этих процессов служат интенсивные боли тянущего характера в нижних отделах живота. Они могут продолжаться несколько часов и очень хорошо откликаются на обезболивающие препараты.
Помимо болей в первые часы могут появиться и другие последствия эмболизации маточных артерий: умеренная лихорадка, слабость, тошнота и/или рвота, недомогание и прочие. Эти клинические проявления называются постэмболизационным синдромом и считаются физиологическими, так как означают период адаптации организма и не приносят вреда здоровью. Они хорошо купируются с помощью лекарств, продолжаются недолго и бесследно самостоятельно исчезают.
Пребывание в стационаре в отсутствии осложнений ограничивается тремя днями, а затем пациентка возвращается домой. Перед тем, как отпустить пациентку из клиники, врач проводит контрольное ультразвуковое исследование и назначает время для повторных осмотров, обычно их проводят спустя 2 недели, а затем повторяют через 3, 6 и 12 месяцев. Также пациентке объясняют, как купировать симптомы постэмболизационного синдрома самостоятельно.
Самым активным периодом регресса миоматозных узлов являются первые полгода после эмболизации. В среднем через год размеры узлов миомы уменьшаются в 4 раза, а величина матки возвращается к нормальным значениям. На характер и скорость регрессии миоматозных узлов влияет их размер и локализация. Расположенные по задней стенке узлы миомы регрессируют в меньшей степени. Субмукозные узлы, расположенные очень близко к полости матки, могут самостоятельно «отрываться» и выходить наружу («экспульсия»).
Не должны пугать пациентку межменструальные кровянистые выделения после эмболизации маточных артерий, если они носят временный характер и не имеют тенденции к усугублению. Менструальный цикл возвращается в прежнее состояние через три месяца после процедуры.
Негативные последствия эмболизации маточных артерий чаще связаны с погрешностями ее исполнения. Если процедура проводится грамотным хирургом с использованием подходящей аппаратуры, процент осложнений очень мал (2%).