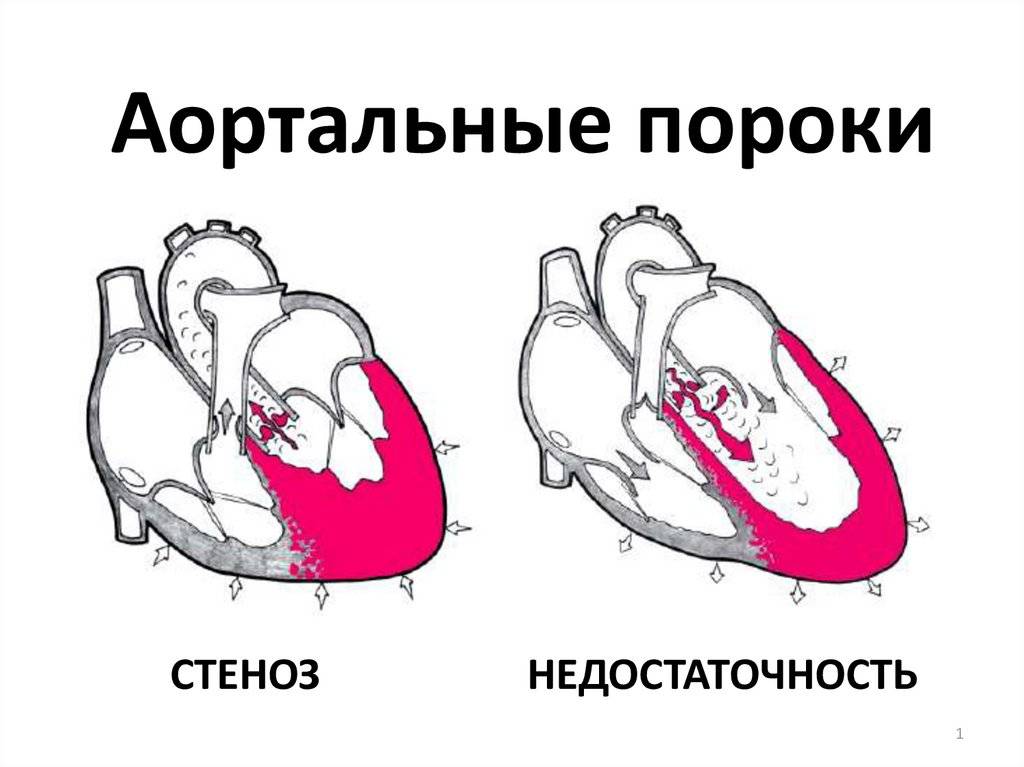
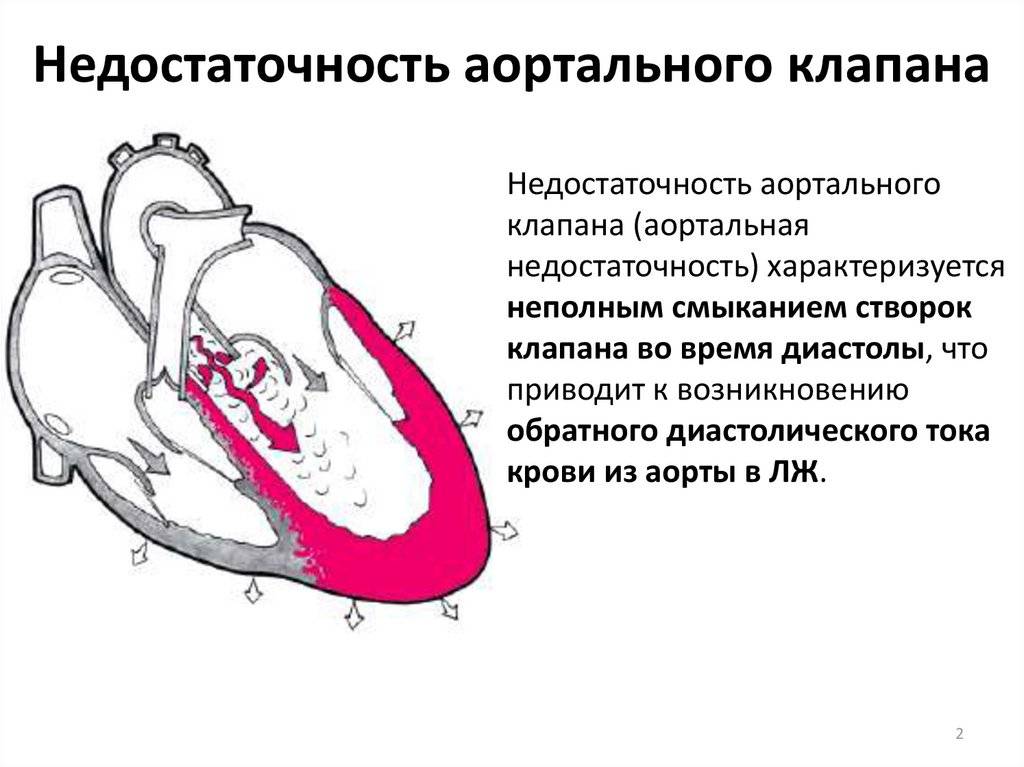
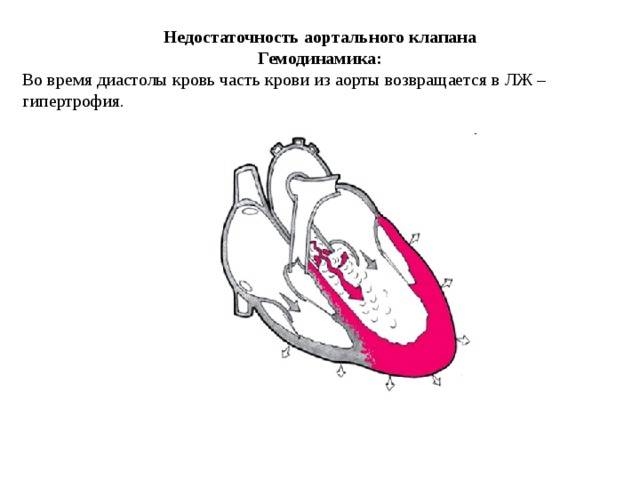
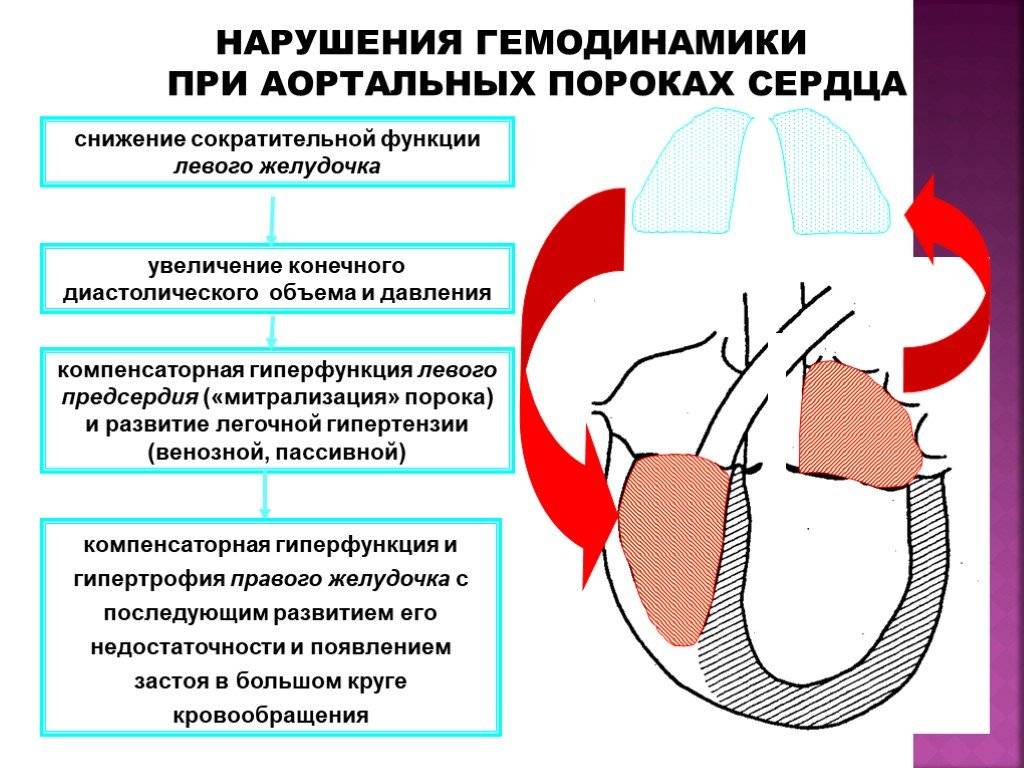
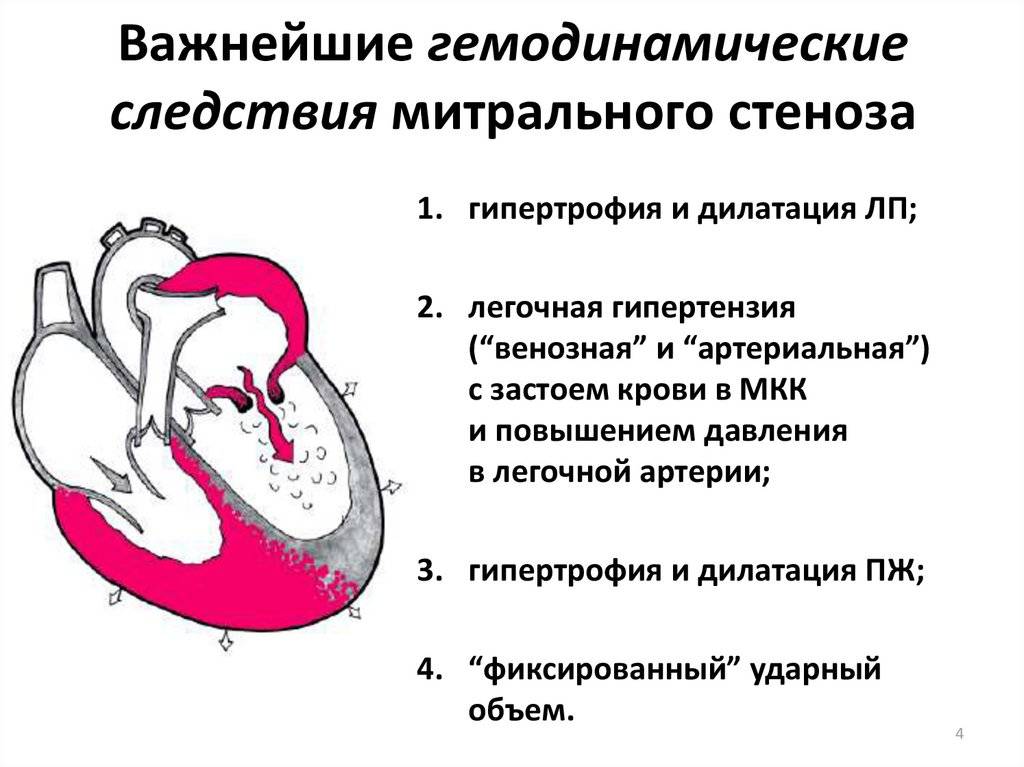
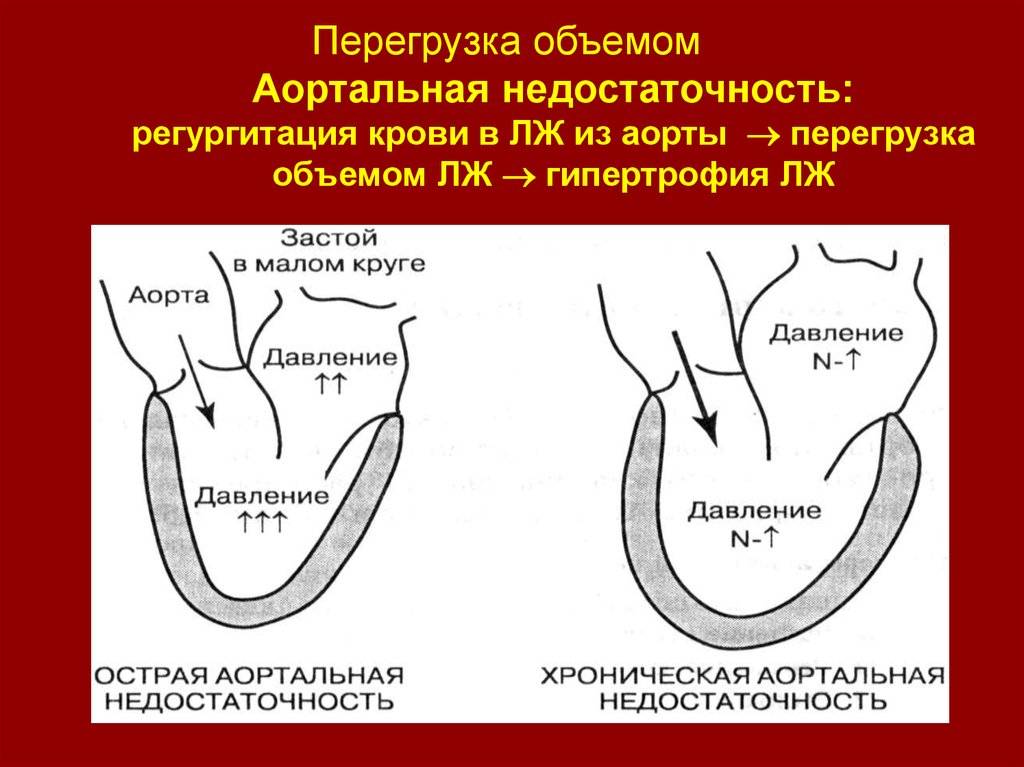
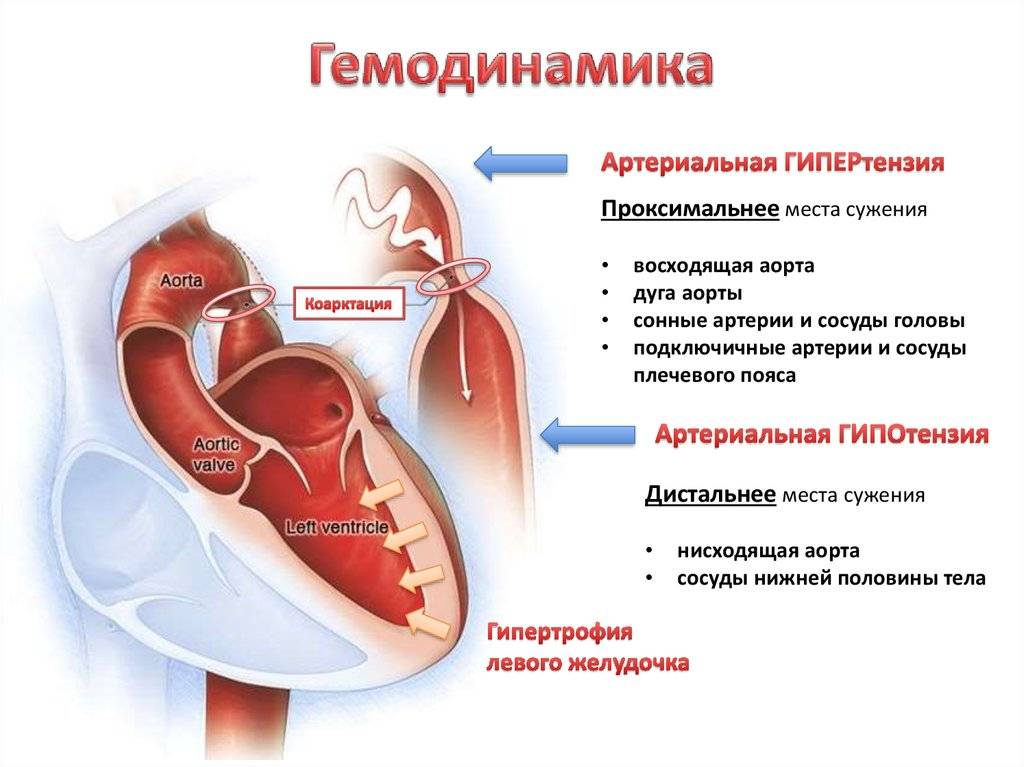
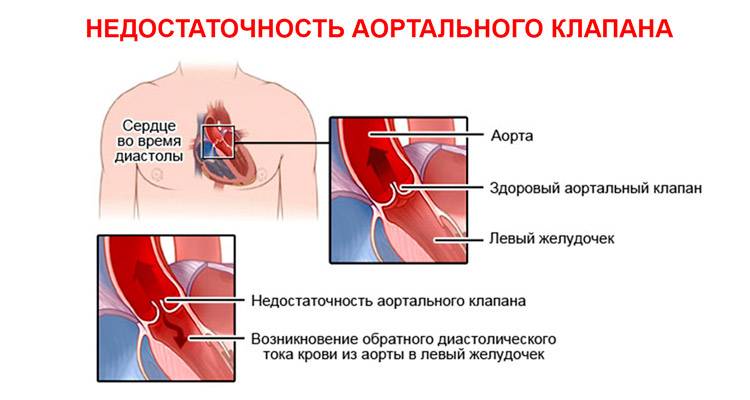
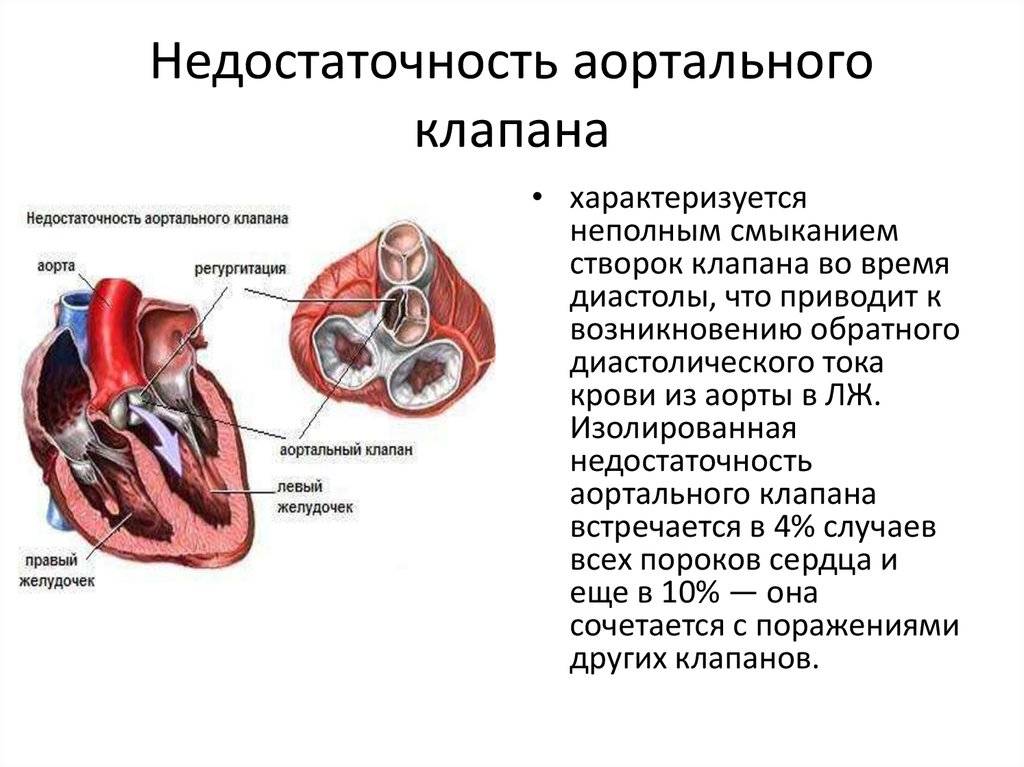
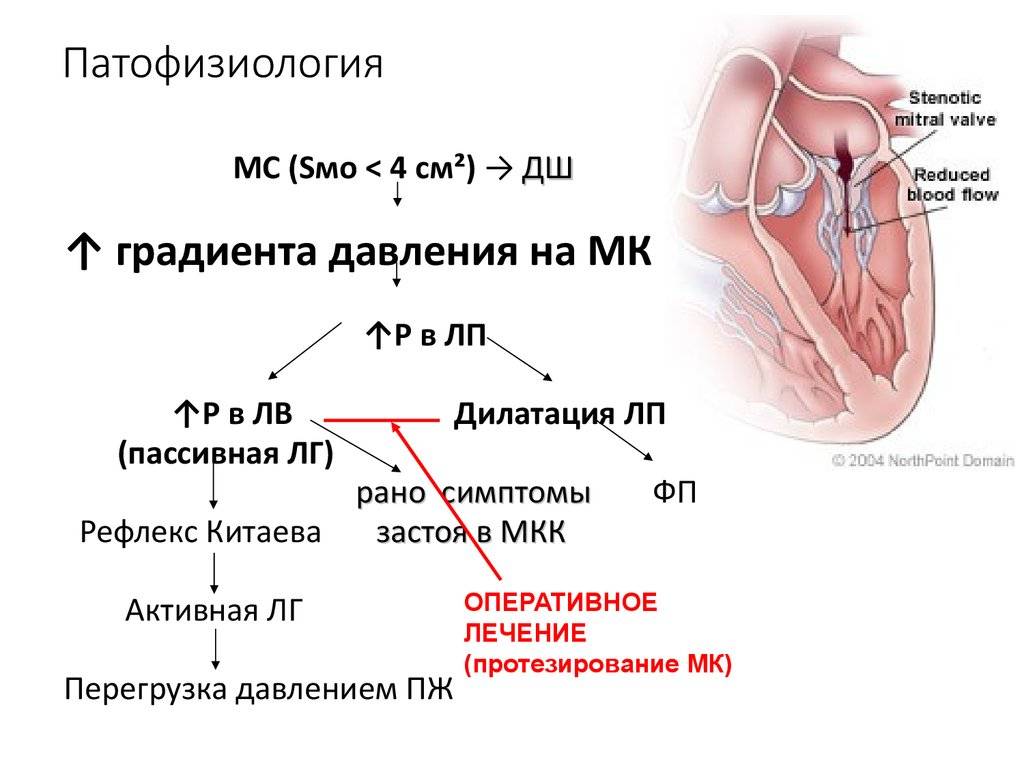
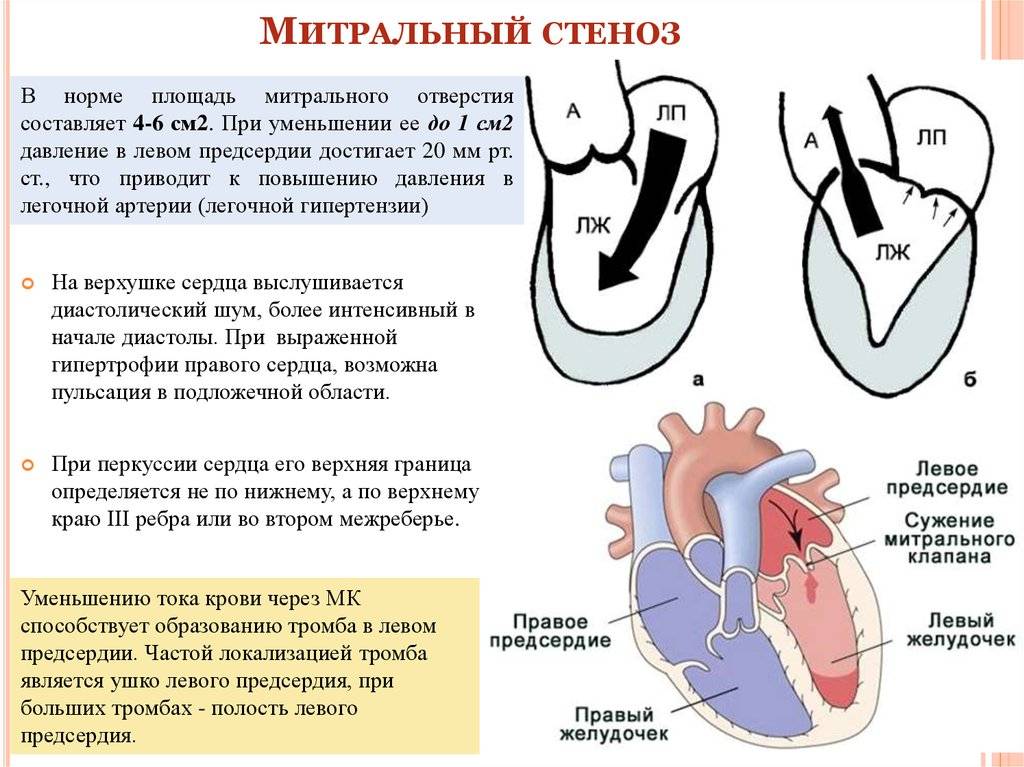
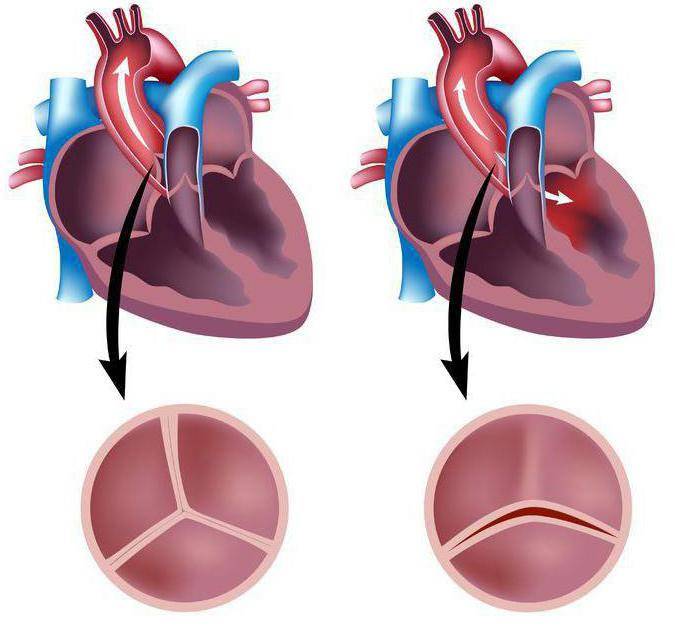
Особенности у детей
Причинами порока митральный стеноз у детей могут быть системные аутоиммунные заболевания:
- Ревматизм.
- Дерматомиозит.
- Системная красная волчанка.
- Полимиозит.
 В подавляющем большинстве случаев этиологией порока у ребенка являются непролеченная ангина и отсутствие бициллинопрофилактики после стрептококковой инфекции.
В подавляющем большинстве случаев этиологией порока у ребенка являются непролеченная ангина и отсутствие бициллинопрофилактики после стрептококковой инфекции.
Заболевание характеризуется теми же гемодинамическими изменениями, что и у взрослых, однако в клинике имеются некоторые особенности:
- Отставание в физическом развитии.
- «Митральное лицо» развивается редко.
- Болезнь не осложняется фибрилляцией предсердий.
- «Ритм перепела» выслушивается редко, более характерны протодиастолический и предиастолический шумы на верхушке сердца.
Особые симптомы:
- Частые обмороки.
- Выраженная эпигастральная пульсация (вплоть до развития «сердечного горба»).
Способы лечения:
- Консервативный (подготовка к операции)
- Оперативный (протезирование клапана).
Прогноз без лечения неблагоприятный. Операция проводится в первый месяц после постановки диагноза и завершается успешно более, чем в 90% случаев. Продолжительность жизни пролеченных больных – 55-65 лет.
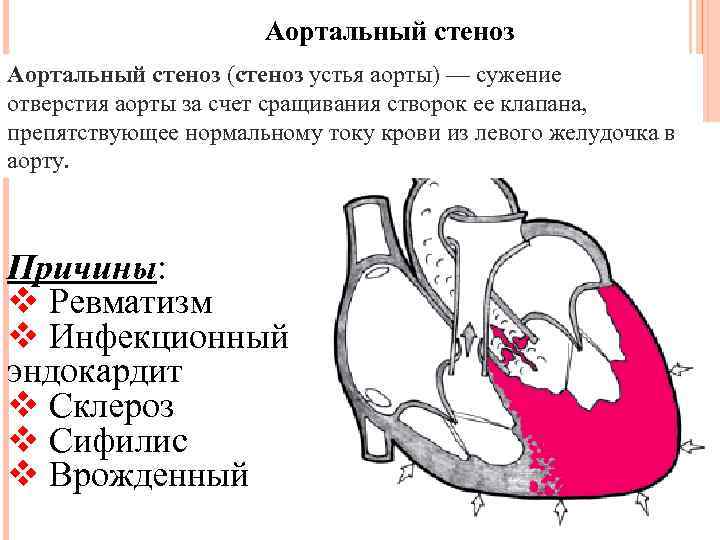
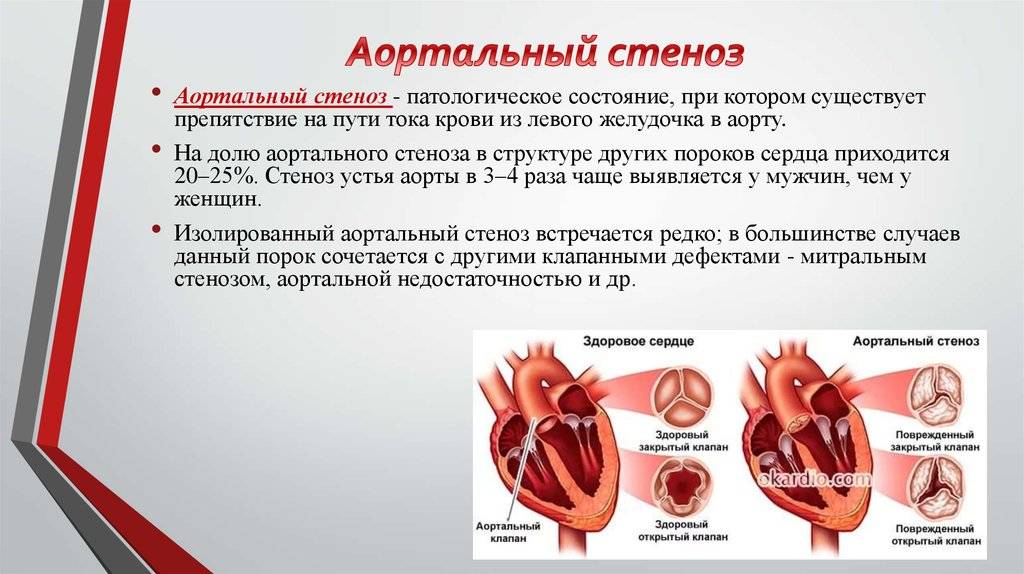
Причины
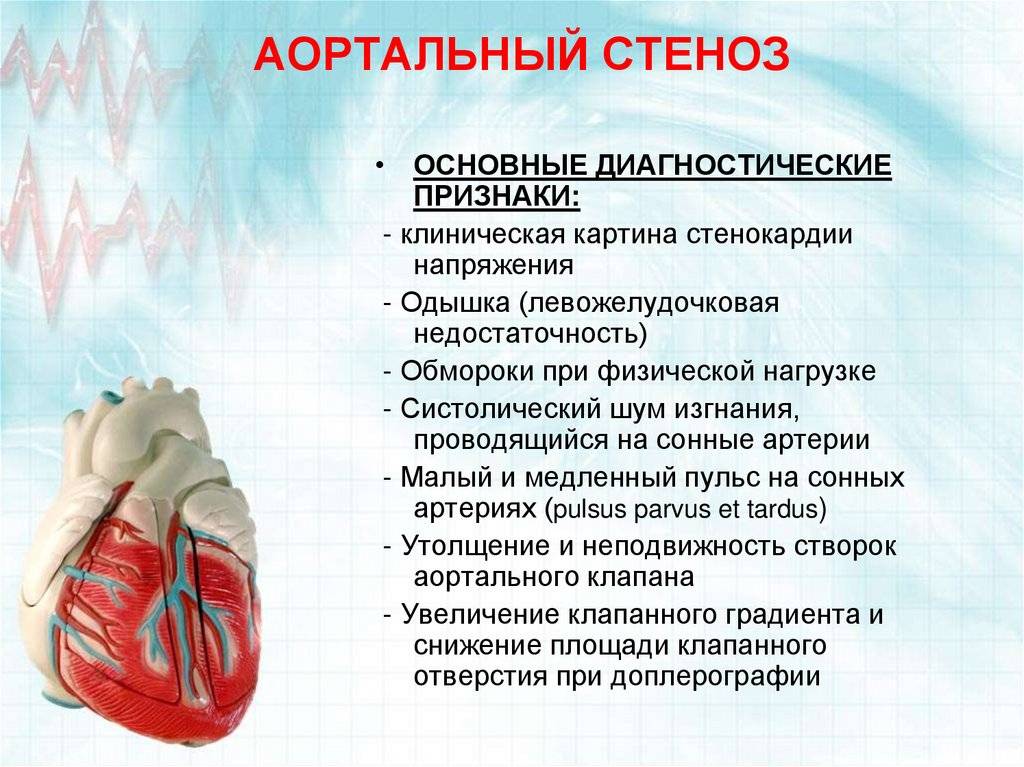
Врожденный клапанный аортальный стеноз
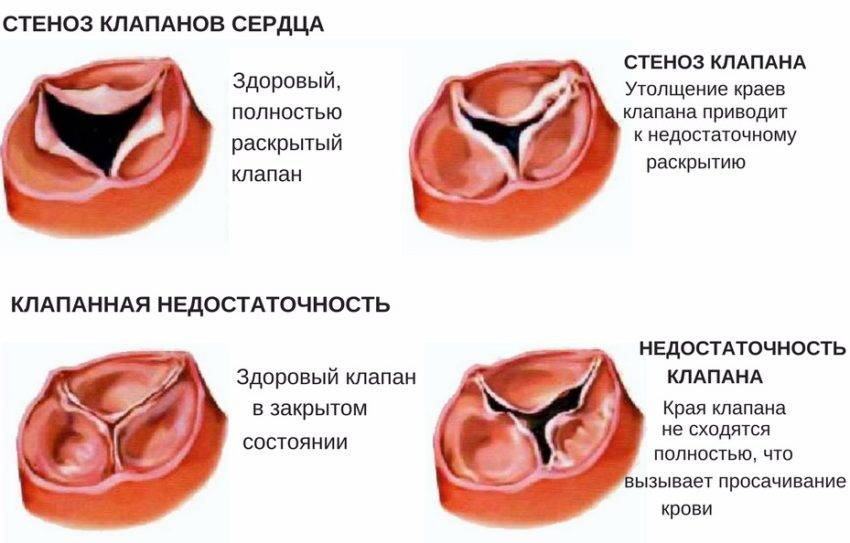
Врожденно односторонние, двустворчатые, трехстворчатые или даже четырехугольные клапаны могут вызывать стеноз аорты. У новорожденных и детей младше 1 года одностворчатый клапан может вызывать тяжелую обструкцию и является наиболее распространенной аномалией у детей с фатальным клапанным стенозом аорты. У пациентов моложе 15 лет односторонние клапаны наиболее часты в случаях симптоматического аортального стеноза.
У взрослых, у которых развиваются симптомы врожденного аортального стеноза, обычно проблема заключается в двустворчатом клапане. Двустворчатые клапаны не вызывают значительного сужения отверстия аорты в детском возрасте. Измененная архитектура двустворчатого аортального клапана вызывает турбулентный поток с непрерывной травмой к листочкам, что в конечном итоге приводит к фиброзу, повышенной жесткости и кальцификации листочков и сужению отверстия аорты в зрелом возрасте.
Когортное исследование, проведенное среди 642 взрослых амбулаторных пациентов с двустворчатыми аортальными клапанами, показало, что в течение средней продолжительности наблюдения 9 лет показатели выживаемости были не ниже, чем в общей популяции. Тем не менее, молодые люди с двустворчатым аортальным клапаном имели высокую вероятность того, что в конечном итоге потребуется вмешательство аортального клапана.
Врожденно деформированные трехстворчатые аортальные клапаны с острыми шипами неравномерного размера и спаечным слиянием («функционально двустворчатые» клапаны) также могут вызывать турбулентное течение, приводящее к фиброзу и, в конечном итоге, к кальцификации и стенозу. Клинические проявления врожденного аортального стеноза у взрослых обычно появляются после четвертого десятилетия жизни.
Приобретенный клапанный аортальный стеноз
Основными причинами приобретенного аортального стеноза являются дегенеративная кальцификация и, реже, ревматическая болезнь сердца.
Дегенеративный кальцинозный аортальный стеноз (также называемый старческим кальцинозным аортальным стенозом) включает в себя прогрессивную кальцификацию тел створки, что приводит к ограничению нормального раскрытия створки во время систолы. Это является следствием давней гемодинамической нагрузки на клапан и в настоящее время является наиболее частой причиной аортального стеноза, требующего замены аортального клапана. Кальцификация может также включать митральное кольцо или проходить в проводящую систему, что приводит к дефектам атриовентрикулярной или внутрижелудочковой проводимости.
Факторы риска дегенеративного кальцинозного аортального стеноза включают пожилой возраст, гипертонию, гиперхолестеринемию, сахарный диабет и курение. Имеющиеся данные свидетельствуют о том, что развитие и прогрессирование заболевания обусловлены активным процессом заболевания на клеточном и молекулярном уровне, который демонстрирует много сходства с атеросклерозом, начиная от эндотелиальной дисфункции и заканчивая, в конечном счете, кальцификацией.
При ревматическом аортальном стенозе лежащий в основе процесс включает прогрессирующий фиброз створок клапана с различной степенью спаечного слияния, часто с втягиванием краев створки и, в некоторых случаях, кальцификацией. Как следствие, ревматический клапан часто бывает срыгивающим и стенотическим. Сосуществующее заболевание митрального клапана является распространенным явлением.
Другие, нечастые причины аортального стеноза включают обструктивные вегетации, гомозиготную гиперхолестеринемию II типа, болезнь Педжета, болезнь Фабри, хроноз и облучение.
Стоит отметить, что, хотя часто проводится дифференциация между стенками трехстворчатого и двустворчатого аортального клапана, часто трудно определить количество створок аортального клапана. Исследование, сравнивающее оперативно вырезанную оценку структуры аортального клапана кардиохирургами и патологами, обнаружило, что определение структуры клапана часто было несоответствующим.
Осложнения
Отсутствие лечения приводит к необратимым осложнениям и поражениям внутренних органов ребёнка, вплоть до летального исхода.
Поскольку организм малыша постоянно растёт, сердце также увеличивается в размерах, в связи с чем операцию на сердце приходится неоднократно повторять. Ребёнок находится на пожизненном наблюдении у кардиолога и кардиохирурга.
Что можете сделать вы
Несмотря на то, что лёгкие стадии недостаточности не оказывают отрицательного влияния на здоровье ребёнка, важно направлять его на осмотр к соответствующему специалисту для исключения и предотвращения осложнений. Тяжёлые формы требуют немедленного врачебного вмешательства
Что делает врач
Поскольку зачастую митральная недостаточность выступает в качестве осложнения какого-либо причинного заболевания, для восстановления функции клапана важно устранить эту болезнь. Бессимптомное течение хронической стадии данного заболевания не нуждается в назначении особых лечебных мер
Остальные стадии болезни подразумевают приём специальных препаратов, в задачи которых входит:
Бессимптомное течение хронической стадии данного заболевания не нуждается в назначении особых лечебных мер. Остальные стадии болезни подразумевают приём специальных препаратов, в задачи которых входит:
- поддержание/стабилизация ритмов сердца;
- предотвращение/лечение недостаточности кровообращения.
Консервативная терапия не даёт должного эффекта в случае поздних стадий недостаточности, чем объясняется необходимость проведения хирургических операций (пластических или с использованием протеза).
Лечение
 В обязательном порядке необходимо лечение основного заболевания, которое привело к возникновению порока.
В обязательном порядке необходимо лечение основного заболевания, которое привело к возникновению порока.
На ранних стадиях заболевания назначают лекарственные препараты, которые помогают насытить сердце кислородом, нормализуют кровообращение и защищают миокард от быстрого истощения. Для этого используют:
- Антагонисты кальция (Верапамил, Анипамил и др.) – эти препараты препятствуют попаданию кальция в клетки сердца, что замедляет сердцебиение и дает миокарду дополнительный отдых. Кроме того, они расширяют сосуды и понижают артериальное давление.
- Мочегонные препараты (Фуросемид, Торасемид и др.) – с их помощью лишняя вода выходит из организма, благодаря чему уменьшаются отеки и снижается нагрузка на сердце. Как следствие понижается артериальное давление и потребность сердца в кислороде.
- Бета-адреноблокаторы (Пропранолол, Метопролол и др.) – эти препараты блокируют чувствительные к адреналину рецепторы. Это позволяет уменьшить частоту сердечных сокращений и снизить артериальное давление. Потребность миокарда в кислороде также снижается.
- Вазодилататоры (гидралазин, диазоксид и др.) – снимают спазм мелких артерий и снижают давление на стенки сосудов, тем самым улучшая кровообращение.
- Ингибиторы АПФ – препараты данной группы способствуют расширению сосудов, приводят в норму давление и помогают сердцу работать лучше.
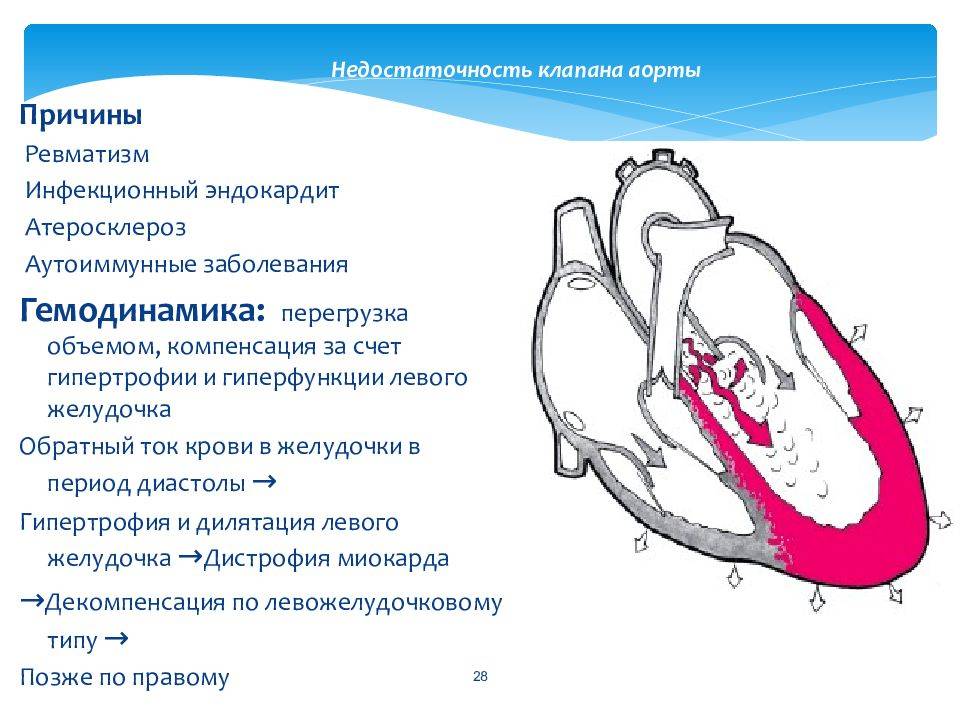
Препараты, которые замедляют сердцебиение, следует с осторожностью назначать при аортальной недостаточности, а также если сочетанный аортальный порок сердца сопровождается более выраженной недостаточностью аортального клапана, поскольку они могут способствовать увеличению объема крови, который возвращается из аорты в левый желудочек. Случаи, в которых стоит прибегнуть к хирургическому лечению:
Случаи, в которых стоит прибегнуть к хирургическому лечению:
- Выраженные симптомы, нарушающие жизнедеятельность пациента;
- Сильное увеличение левого желудочка;
- При аортальной недостаточности из аорты возвращается около 50% крови;
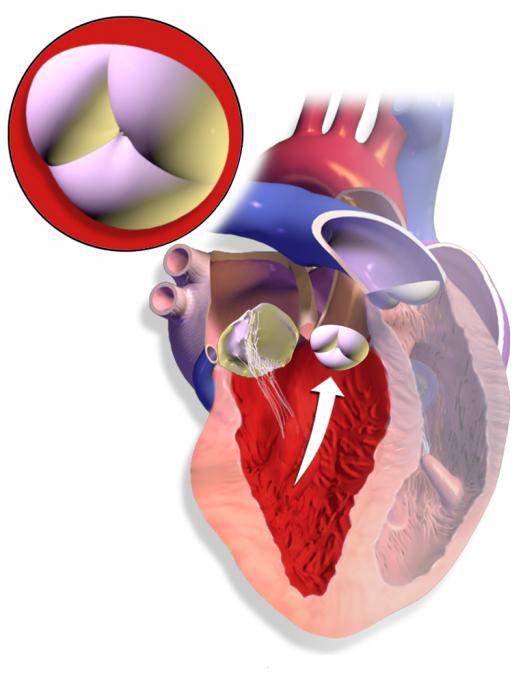
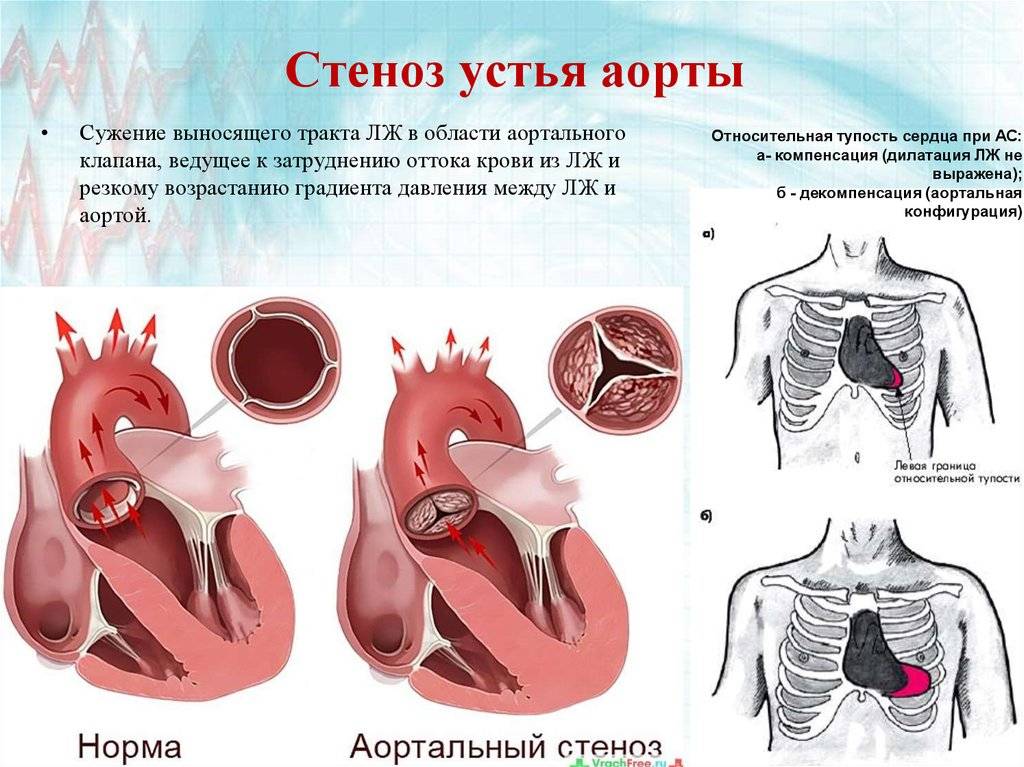
- Если при стенозе устья аорты просвет составляет меньше 1,5 кв. см.
Если порок врожденный, операции обычно не проводят до тридцати лет, однако, при выраженных симптомах и быстром прогрессировании заболевания могут проводиться и раньше. Хирургические вмешательства не назначают пациентам, которым больше семидесяти лет и которые имеют другие тяжелые заболевания.
Виды хирургических операций:
- Внутриаортальная баллонная пластика – через бедренную артерию в полость сердца вводится специальный баллон. Когда он достигает аортального клапана, с помощью гелия его раздувают. Это увеличивает отверстие при стенозе устья аорты и выравнивает створки, чтобы они лучше смыкались при аортальной недостаточности. Делают такую операцию лишь на ранних стадиях развития болезни. Ее недостатком является то, что через какое-то время порок может развиться снова.
- Протезирование клапана. Вместо поврежденного аортального клапана устанавливается искусственный. Он может быть либо синтетическим, то есть созданным из силикона и металла, либо биологическим, человеческого или животного происхождения. Последний используют очень редко. Протезирование клапана может проводиться во время операции на открытом сердце или с доступом через бедренную артерию. Второй способ представляет собой эндоваскулярное протезирование аортального клапана, не требует общего наркоза и является малоинвазивным.
- Пересадка сердца – проводится по исключительным показаниям, когда собственное сердце человека крайне изношено и не поддается лечению.
Прогнозы и выживаемость
Если диагностировать недуг на начальной стадии, то после проведения операции 5-летний прогноз выживаемости будет равен 85%, 10-летний – 70%. Если болезнь находится в запущенной стадии, то прогноз сокращается до 5-8 лет жизни. У новорожденных детей смерть наблюдают в 10% случаев.
Если площадь отверстия сосуда находится в пределах до 30%, то больной чувствует себя достаточно удовлетворительно и может многие годы обходится просто под наблюдением кардиолога. Большую роль играет возраст больного — чем моложе пациент, тем больше у него шансов на нормальную длительную и полноценную жизнь.
Изолированный аортальный стеноз при условии должного лечения дает благоприятный прогноз на будущее. Больные с таким заболеванием могут долго оставаться трудоспособными, ограничив при этом свои физические нагрузки.
 Оперативное вмешательство при этой патологии практически всегда гарантирует благоприятный исход. Смертность даже при тяжелой степени заболевания у ослабленных пациентов не превышает в данном случае 10%.
Оперативное вмешательство при этой патологии практически всегда гарантирует благоприятный исход. Смертность даже при тяжелой степени заболевания у ослабленных пациентов не превышает в данном случае 10%.
Всем пациентам, вне зависимости от методов и результатов лечения, необходимо пересмотреть свой образ жизни в пользу:
- ограничения физического труда;
- отказа от вредных привычек;
- бессолевой диеты.
Это является лучшей профилактикой рецидива заболевания и резкого ухудшения состояния больного.
Общие сведения
Митральный клапан – это две соединительнотканные пластинки, расположенные между предсердием и желудочком левой части сердца. Данный клапан:
- препятствует возникающему при сокращении желудочков обратному току крови (регургитации) в левое предсердие;
- отличается овальной формой, размер в поперечнике колеблется от 17 до 33 мм, а продольный составляет 23 – 37 мм;
- обладает передней и задней створками, при этом передняя лучше развита (при сокращении желудочка выгибается по направлению к левому венозному кольцу и совместно с задней створкой закрывает это кольцо, а при расслаблении желудочка закрывает аортальное отверстие, прилегая к межжелудочковой перегородке).
Задняя створка митрального клапана шире передней. Распространены вариации числа и ширины частей задней створки — может делиться на латеральную, среднюю и медиальную фалды (наиболее длинной является средняя часть).
Возможны вариации расположения и количества хорд.
При сокращении предсердия клапан находится в открытом состоянии и в желудочек в этот момент поступает кровь. При наполнении желудочка кровью клапан закрывается, желудочек сокращается и выталкивает кровь в аорту.
При изменении сердечной мышцы или при некоторых патологиях соединительной ткани строение митрального клапана нарушается, в результате чего при сокращении желудочка створки клапана прогибаются в полость левого предсердия, пропуская часть поступившей в желудочек крови обратно.
Патологию впервые описали в 1887 г. Cuffer и Borbillon как аускультативный феномен (выявляется при выслушивании сердца), проявляющийся в виде среднесистолических кликов (щелчков), которые не связаны с изгнанием крови.
В 1892 году Griffith выявил связь апикального позднесистолического шума с митральной регургитацией.
В 1961 году J. Reid опубликовал работу, в которой убедительно показал связь среднесистолических щелчков с тугим натяжением расслабленных хорд.
Выявить причину позднего шума и систолических щелчков удалось только при ангиографическом обследовании больных с указанной звуковой симптоматикой (проводилось в 1963- 1968 гг. J. Barlow с коллегами). Проводившие обследование специалисты обнаружили, что при данной симптоматике во время систолы левого желудочка происходит своеобразное провисание створок митрального клапана в полость левого предсердия. Выявленное сочетание баллоновидной деформации створок митрального клапана с систолическим шумом и щелчками, которое сопровождается характерными электрокардиографическими проявлениями, авторы обозначили как аускультативно-электрокардиографический синдром. В процессе дальнейших исследований этот синдром стали называть синдромом щелчка, синдромом хлопающего клапана, синдромом щелчка и шума, синдромом Barlow, синдромом Энгла и др.
Наиболее распространенный термин «пролапс митрального клапана» впервые был использован J Criley.
Хотя принято считать, что пролапс митрального клапана чаще всего наблюдается у лиц молодого возраста, данные Фремингемского исследования (самого продолжительного эпидемиологического исследования в истории медицины, которое длится 65 лет) показывают, что существенной разницы во встречаемости этого нарушения у лиц различных возрастных групп и пола нет. Согласно данным этого исследования, данная патология встречается у 2.4 % людей.
Частота выявленного пролапса у детей составляет 2-16% (зависит от метода его выявления). У новорожденных наблюдается редко, чаще обнаруживается в 7-15 лет. До 10 лет патология одинаково часто наблюдается у детей обоих полов, но после 10 лет чаще выявляется у девочек (2:1).
При наличии кардиальной патологии у детей пролапс выявляется в 10-23% случаев (высокие значения наблюдаются при наследственных заболеваниях соединительной ткани).
Установлено, что при небольшом возврате крови (регургитации) эта самая распространенная клапанная патология сердца никак себя не проявляет, отличается хорошим прогнозом и в лечении не нуждается. При значительной величине обратного потока крови пролапс может представлять опасность и требует хирургического вмешательства, так как у некоторых пациентов развиваются осложнения (сердечная недостаточность, разрыв хорд, инфекционный эндокардит, тромбоэмболия с миксоматозным изменением митральных створок).
Диагностика
Надежным способом распознавания пролапса сердечного клапана любой степени у ребенка служит ультразвуковое исследование – эхокардиография. Метод дает возможность определить степень выбухания клапана в предсердие и величину заброса.
Осмотр больных, выслушивание сердца являются решающими способами диагностики при патологии сердечного клапана. Признаком выпячивания клапана в предсердие при сокращении желудочков служит щелчок, сопровождающийся позднесистолическим шумом. Щелчки становятся более четко различимыми при нагрузке и в вертикальном положении.
Инструментальную диагностику проводят с помощью:
- Эхокардиографии;
- ЭКГ;
- Холтеровского мониторирования;
- Рентгенографии;
- Катетеризации.
Методы:
- Фонокардиография. Способ позволяет выяснить происхождение шумов в органе.
- Узи сердца. Показывает строение органа и нарушения в его структуре изнутри.
- ЭКГ (электрокардиограмма) применяется для выявления нарушений проводимости органа и его ритма.
- Рентгенологическое обследование сердца, которое необходимо для оценки состояния, размеров и других особенностей органа.
- Холтеровское мониторирование тоже применяется для обнаружения электрокардиографических расстройств.
- Доплер-ЭхоКГ помогает врачу выявить изменения в тканях клапана и всей клапанной системы, позволяет оценить степень прогиба створок, насколько выражена регургитация, а также масштабы нарушений гемодинамики органа.
- Психологические тесты и обследование функционирования центральной нервной системы позволяют определить наличие вегетативных расстройств.
Помимо этих методов диагностики, врачи могут назначить проведение лабораторных исследований, анализы крови, позволяющие обнаружить воспалительный процесс в организме малыша.
Диагностика и лечение
Магнитно-резонансная томография
Основными методами диагностики ГЛЖ являются эхокардиография (УЗИ сердца), магнитно-резонансная томография и другие методы. Однако, в самом начале весь диагностический поиск направлен на установление основного заболевания. Первыми жалобами пациента с ГЛЖ могут быть одышка, которую он испытывает при выполнении интенсивных физических нагрузок. При прогрессировании процесса данный симптом может проявляться и в момент выполнения нагрузок меньшей интенсивности, а после и в покое. Последний момент указывает на развитие у пациента сердечной недостаточности (СН).
Кроме одышки, пациенты предъявляют жалобы, касающиеся основного заболевания. Могут беспокоить болевые ощущения или дискомфорт в области сердца или за грудиной, которые имеют связь с нагрузками или стрессами. Также могут присутствовать сердцебиение, головокружение, головные боли, обморочные состояния. Список симптомов может быть дополнен ощущениями перебоев в работе сердца, повышенной утомляемостью, слабостью и другими признаками основного заболевания.
Эхокардиография сердца
Ведущим инструментальным методом гипертрофии миокарда левого желудочка является эхокардиография (ЭхоКГ или УЗИ сердца). Несмотря на то, что такой простой и доступный метод инструментальной диагностики как электрокардиография (ЭКГ) также имеет свои диагностические критерии в отношении ГЛЖ, все же, УЗИ сердца по своей диагностической чувствительности превосходит ЭКГ более чем в 5 раз. Основным эхокардиографическим показателем, который учитывается при постановке диагнозе ГЛЖ, является масса миокарда левого желудочка (ММЛЖ), а точнее ее индекс.
Для разграничения концнтрического или эксцентрического ремоделирования используется также такой эхокардиографический показатель как относительная толщина стенки (ОТС). В зависимости от состояния этих двух показателей — ИММЛЖ и ОТС, определяется тип ремоделирования миокарда ЛЖ:
- Нормальная геометрическая структура левого желудочка выставляется при том условии, если ОТС менее 0,45; а ИММЛЖ находится в пределах нормы.
- Концентрическое ремоделирование имеет следующие эхокардиографические критерии: ОТС равно или меньше 0,45; ИММЛЖ при этом остается нормальным.
- Эксцентрическое ремоделирование характеризуется ОТС менее 0,45 при ИММЛЖ больше нормы.
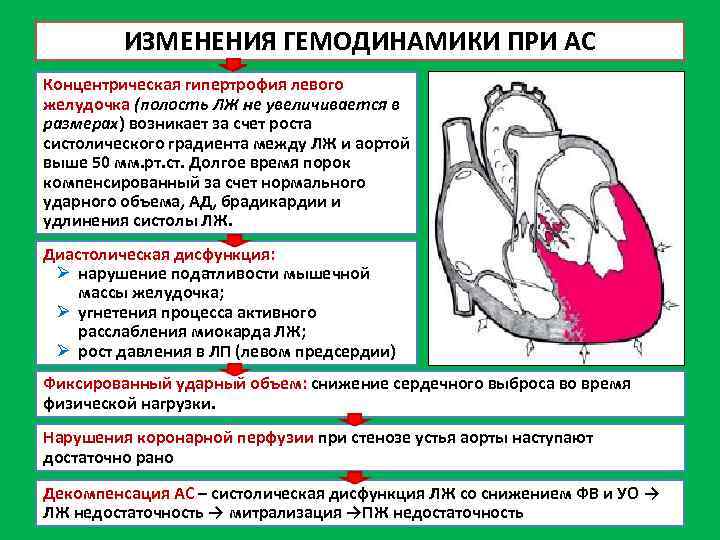
Диастолическая дисфункция
Прогностически более неблагоприятной считается концентрическая гипертрофия ЛЖ, так как именно этот тип ремоделирования миокарда влечет за собой диастолическую дисфункцию и электрическую нестабильность миокарда, повышая тем самым риск развития внезапной сердечной смерти среди таких пациентов. На выраженность диастолической диасфункции независимо от типа гипертрофии влияет относительная толщина стенки. Чем больше степень ее увеличения, тем неблагоприятнее прогноз. А вот возрастание конечно-диастолического разера коррелирует с выраженностью систолической дисфункции ЛЖ.
Нелеченая ГЛЖ может осложняться такими состояниями как аритмии, ишемическая болезнь сердца (ИБС), сердечная недостаточность, фибрилляция желудочков, внезапная сердечная смерть. Лечение гипертрофии ЛЖ включает в себя лечение основного заболевания, по причине которого развилось такое осложнение. Оно включает в себя немедикаментозные меры — устранение факторов риска, а также прием лекарственных препаратов, поддерживающих функцию сердца и препятствующих прогрессированию этого осложнения. Лечение гипертрофии левого желудочка (ГЛЖ) необходимо проводить обязательно, даже если пациент чувствует себя удовлетворительно.
Стентирование коронарных артерий
При неэффективности лекарственной терапии пациентам с нарушенной функцией ЛЖ показано хирургическое лечение. В зависимости от того, какой структурный компонент пострадал, предлагаются следующие оперативные вмешательства:
- Стентирование коронарных артерий, ангиопластика. Такая процедура назначается в случае развития ишемии миокарда.
- Протезирование клапанов сердца. Такая операция может быть показана, если причиной ГЛЖ стали клапанные пороки.
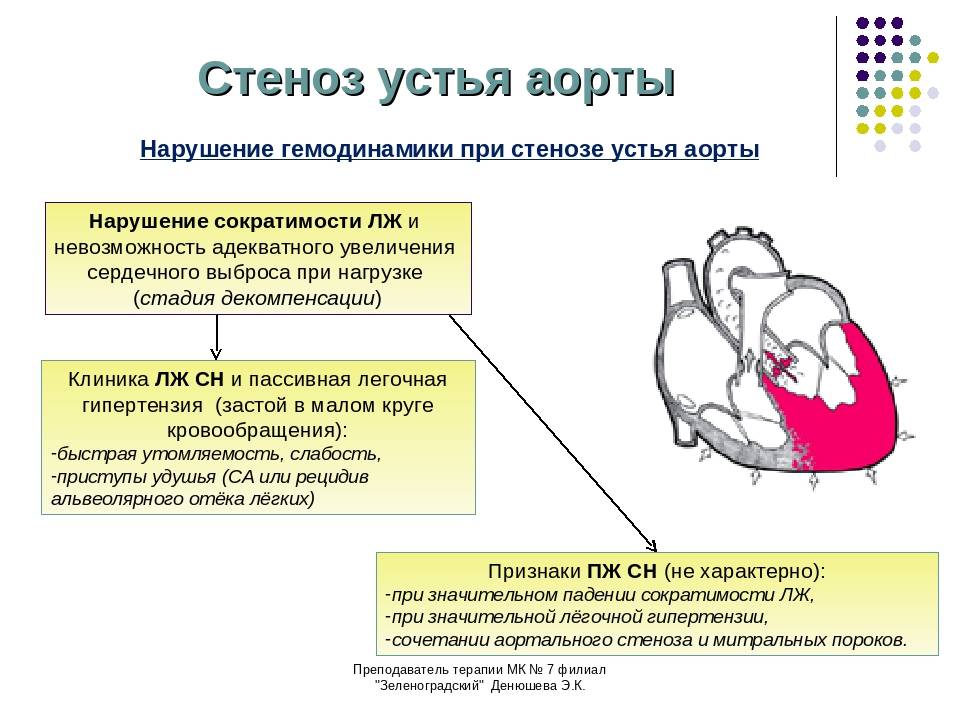
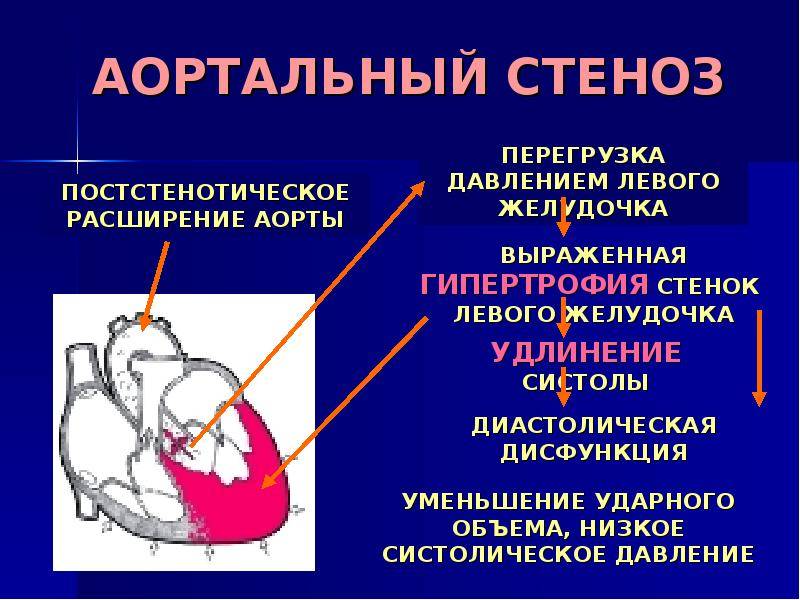
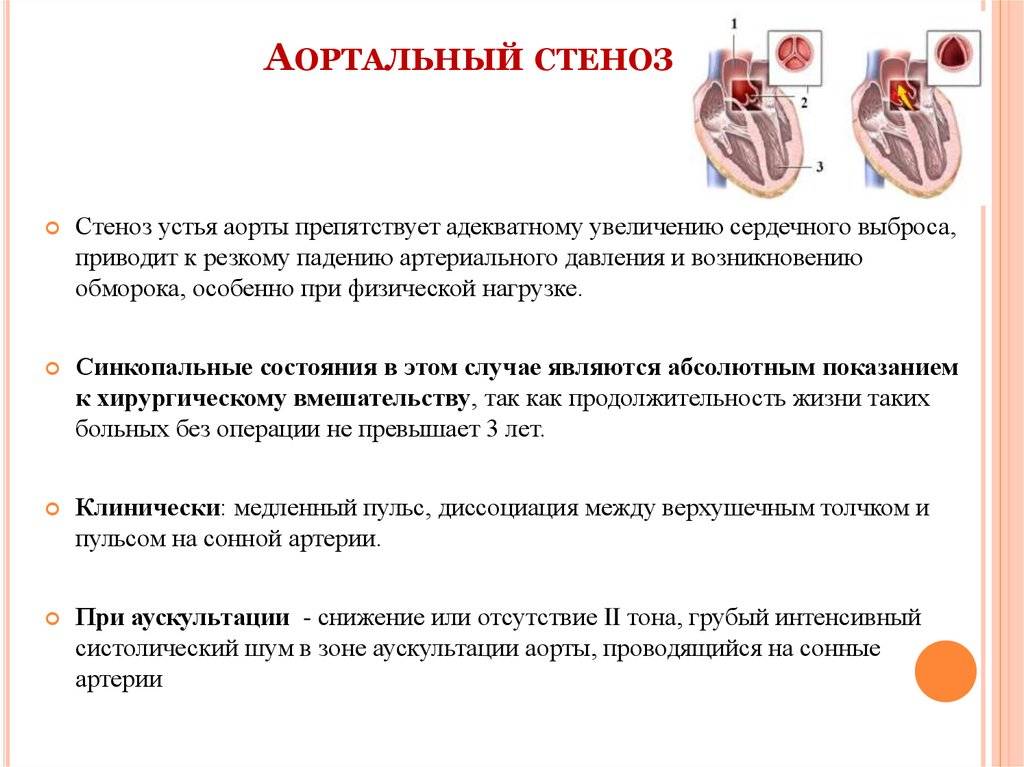
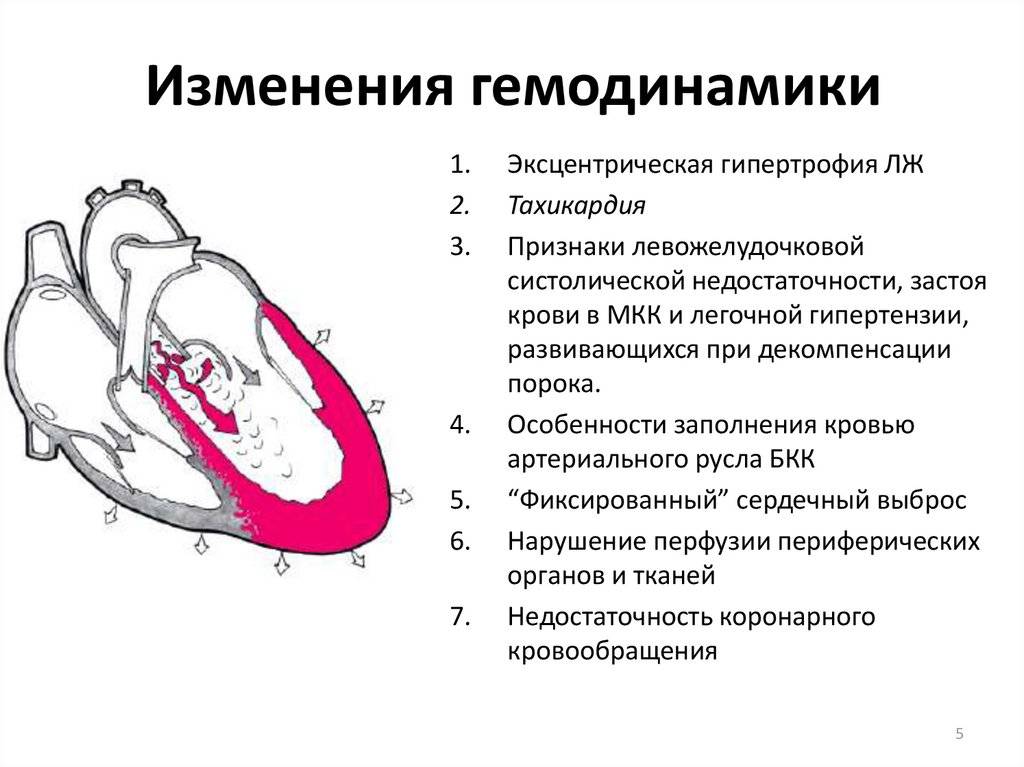
- Рассечение спаек на клапанах (комиссуротомия). Одним из показаний к такому хирургическому вмешательству является стеноз устья аорты. Рассечение комиссур позволяет снизить то сопротивление, которое встречает миокард желудочка при изгнании крови в аорту.
Причины
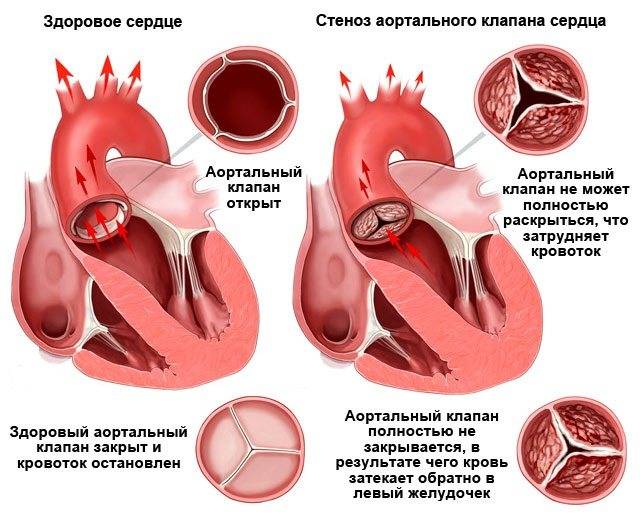
 По отдельности эти пороки могут быть как врожденными, так и приобретенными. Врожденные закладываются еще во время нахождения ребенка в утробе матери. Это может происходить по различным причинам: заболевания беременной женщины, вредные привычки, плохая экология и другие. При этом вместо трех створок могут развиться только две, и тогда аортальный клапан становится двухстворчатым, а не трехстворчатым, что уменьшает просвет, через который проходит кровь. Может быть вообще всего одна створка. Створки могут быть сильно растянуты, что мешает их плотному закрытию, в них могут образовываться отверстия, или над клапаном появляется мышечный валик, мешающий нормальному проходу крови.
По отдельности эти пороки могут быть как врожденными, так и приобретенными. Врожденные закладываются еще во время нахождения ребенка в утробе матери. Это может происходить по различным причинам: заболевания беременной женщины, вредные привычки, плохая экология и другие. При этом вместо трех створок могут развиться только две, и тогда аортальный клапан становится двухстворчатым, а не трехстворчатым, что уменьшает просвет, через который проходит кровь. Может быть вообще всего одна створка. Створки могут быть сильно растянуты, что мешает их плотному закрытию, в них могут образовываться отверстия, или над клапаном появляется мышечный валик, мешающий нормальному проходу крови.
Обычно такие виды сразу не дают явной симптоматики и долгое время о них можно даже не знать. Однако с возрастом пороки проявляют себя и могут потребовать лечения. Сочетанный аортальный порок сердца всегда бывает только приобретенным.
Причины, которые могут вызывать образование пороков:
Различные инфекции (ангина, пневмония, сепсис, сифилис и др.)
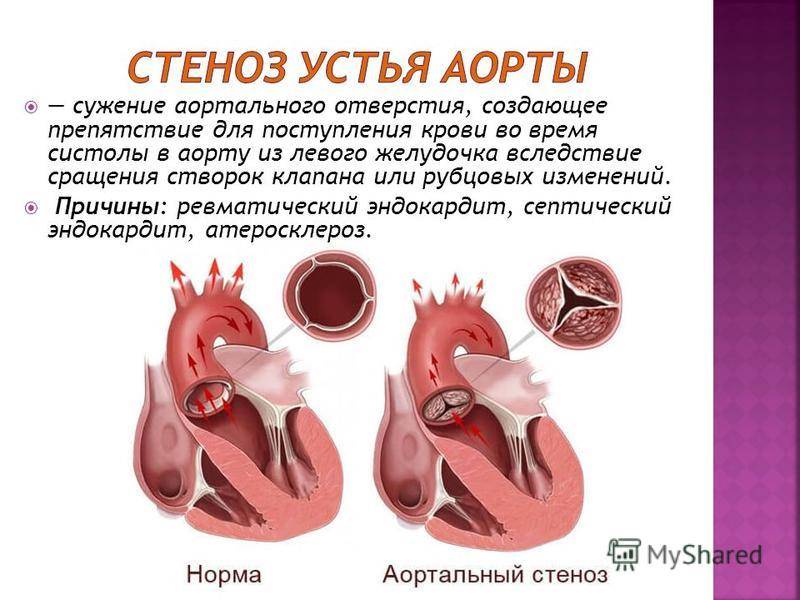
Иногда, особенно при плохом лечении или слишком раннем его прекращении, такие заболевания дают осложнения на сердце. Воспаляется внутренняя его оболочка, что называется инфекционным эндокардитом. Клапаны также состоят из эндокарда, потому бактерии могут скапливаться и на них. Иммунная система организма, защищая его от инфекции, покрывает бактерии лейкоцитами, образуя своеобразные бугорки. Со временем они зарастают соединительной тканью, которая не может растягиваться. Это вызывает стеноз устья аорты и может препятствовать нормальной работе клапанов, не давая им полностью закрыться.
Аутоиммунные заболевания (красная волчанка, ревматизм, склеродермия)
Эти заболевания вызывают сильное разрастание соединительной ткани. Она не позволяет клапанам нормально раскрываться и закрываться, приводит к их изменению и сужению устья аорты, что препятствует продвижению крови по ней. Сочетанный аортальный порок чаще всего вызывается именно ревматизмом.
- Атеросклероз аорты – на внутренней стенке аорты откладывается холестерин и образуются холестериновые бляшки. Постепенно увеличиваясь в размерах, они перекрывают просвет сосуда и мешают нормальному току крови по нему.
- Отложение солей кальция на клапанах.
- Дегенеративные изменения могут быть вызваны также сильным ударом в грудную область, из-за чего может разорваться одна из створок. В этом случае симптомы появляются очень быстро.
- Артериальная гипертензия.
Хирургическое вмешательство
Если медикаментозная терапия не принесла требуемого результата, то для проведения лечения могут назначаться хирургические методики. Показаны такие виды вмешательства как:
- замена митрального клапана;
- операция Морроу;
- комиссуротомия;
- замена или пересадка аортального клапана;
- стентирование коронарных сосудов.
Стентирование назначается в случае ишемии миокарда. При стенозе аорты проводится рассечение спаек на клапанах. Подобная методика позволяет несколько уменьшить сопротивление, которое встречает миокард желудочка при перетекании крови в аорту. Если проведенная терапия не приносит ожидаемого результата, то вшивается кардиовертет-дефибриллятор или электрокардиостимулятор. Эти приборы предназначены для восстановления правильного ритма сердца.
Прогноз
Прогноз протекания болезни определяется первопричиной подобного нарушения. При начальных стадиях гипертрофии, которая корректируется при помощи гипотензивных препаратов, прогноз достаточно хороший. Хроническая форма развивается очень медленно, и человек с такой болезнью может жить на протяжении нескольких десятков лет. При этом качество его жизни не страдает.
У пожилых людей с ишемией миокарда, а также ранее перенесенными инфарктами развитие хронической стадии предсказать достаточно сложно. Она может развиваться как медленно, так и стремительно, что приводит к инвалидности и потере работоспособности человеком.
Причины возникновения
Достаточно часто концентрическая гипертрофия левого желудочка возникает при наличии генетической предрасположенности. Ситуация может усугубиться при ожирении и повышенном давлении. Достаточно часто болезнь развивается по таким причинам, как:
- поражение митрального клапана;
- артериальный стеноз;
- лишний вес;
- высокое давление;
- гипертрофическая кардиомиопатия;
- стресс;
- легочные болезни.
Митральный клапан выполняет регулирование кровообращения в камерах сердечной мышцы. При нарушении его функционирования может развиться гипертрофия. Среди других причин нужно выделить избыточный вес, который приводит к развитию многочисленных нарушений в организме, в том числе и возникновению сердечно-сосудистых патологий.
Зачастую выраженная концентрическая гипертрофия левого желудочка развивается по причине артериальной гипертензии. Нередко к этому состоянию присоединяются также и другие нарушения, которые хорошо просматриваются при проведении электрокардиограммы.
Формирование незначительной концентрической гипертрофии миокарда левого желудочка считается нормой у людей, которые в течение длительного времени профессионально занимаются спортом. При постоянных тренировках нагрузка на сердце оказывается достаточно сильной и постоянной. В результате этого стенки левого желудочка становятся несколько толще.
Несмотря на то что это считается нормой, важно не пропустить момент, когда умеренная концентрическая гипертрофия левого желудочка перейдет в более сложную форму. В связи с этим спортсменов все время находятся под наблюдением врачей, которые точно знают, в каком виде спорта такое состояние допустимо, а в каком его быть не должно
Еще одной причиной образования подобной патологии является ишемия. При этом миокард испытывает периодическую или постоянную нехватку кислорода. Мышечные клетки без дополнительного поступления энергетических субстратов работают не настолько результативно, как это должно быть в норме. Поэтому остальным клеткам приходится функционировать с гораздо большей нагрузкой. Постепенно происходит утолщение сердечной мышцы.
Митральная конфигурация сердца — изменение форм органа, причины и риски для здоровья
Митральная конфигурация сердца – один из вариантов патологической конфигурации. Зачастую возникает при диагнозе митральный стеноз у пациентов. Это отклонение выявляется при прохождении рентгенологического обследования.
Врач при этом в обязательном порядке должен учесть, что на снимках форма сердца является величиной переменой.
Главными факторами, определяющими ее, становится положение тела пациента в пространстве, высота размещения купола и тупость угла диафрагмы в межреберье.
Важно! Контуры сердца имеют половозрастные отличия. Однако нормальная сердечная тень на рентгене межреберья обладает вытянутой овальной формой, расположенной наискось по отношению к ости человеческого тела
Однако нормальная сердечная тень на рентгене межреберья обладает вытянутой овальной формой, расположенной наискось по отношению к ости человеческого тела.
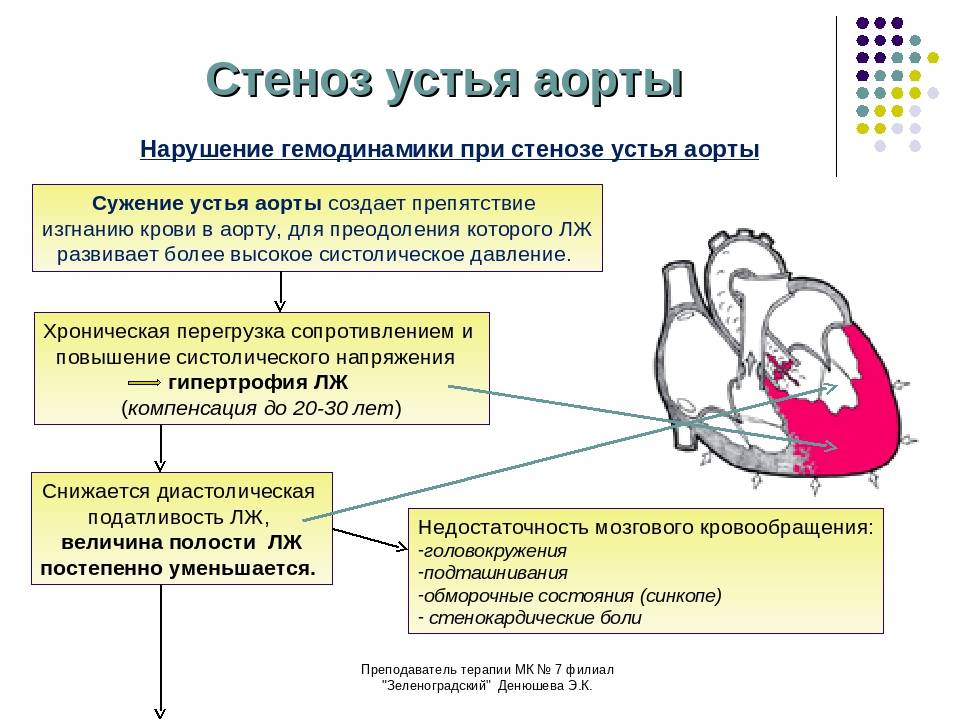
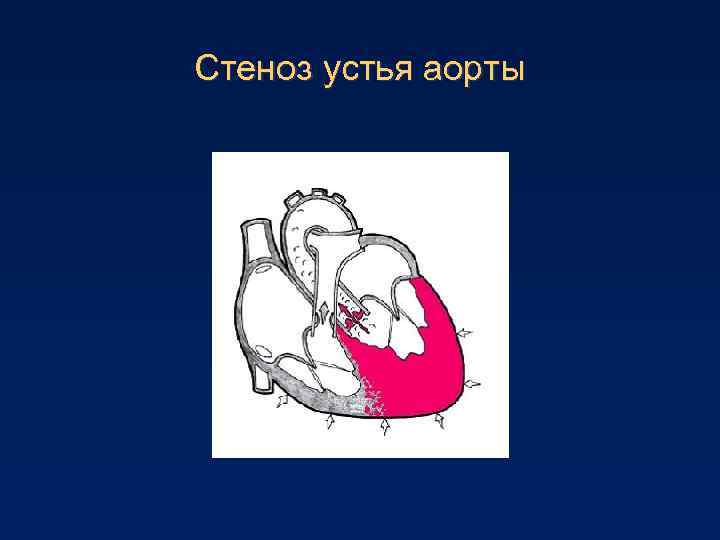
Почему развивается стеноз?
Левое предсердно-желудочковое отверстие сужается из-за:
- Долговременной и сильной перегрузки предсердия и желудочка,
- Ревматизма (текущего либо ранее перенесенного). Но примерно у 20 процентов пациентов с подтвержденной патологией митрального клапана может и не быть ревматизма,
- Врожденной патологии – сужения левого предсердно-желудочкового отверстия. Это заболевание может развиваться на фоне иных, не столь серьезных сердечных пороков,
В случае воспаления эндокарда обычно митральный стеноз не появляется. Однако у некоторых пациентов, получивших неправильное лечение инфекционного эндокардита, возникают признаки несущественно выраженный стеноз с небольшими нарушениями гемодинамики в сердце.
Патологические конфигурации
В рентгенологии выделяют такие патологические нарушения сердечной формы: аортальную, митральную, трапециевидную (контуры описывают треугольник).
Митральная форма
Митральное сердце описывается сглаживанием, тупостью углов, нередко выпуклостью талии сердца, избыточной выпуклостью и увеличением длины третьей и второй дуги слева в межреберье.
Митральная форма сердца образуется при таких патологиях:
- Перегружается правый желудочек при сердечных пороках, хронических легочных заболеваниях,
- Перегружается левое предсердие и желудочек справа из-за стеноза митрального клапана,
- Перегружаются оба желудочка и левая часть предсердия при недостаточности функции митрального клапана.
Аортальная форма
Данный вид конфигурации проявляется в увеличении тупости дуги желудочка с левой границы и выраженными линиями талии сердца посредством западения контура между четвертой и первой дугами. Первая дуга с правой стороны имеет вытянутую в длину форму. Аортальная форма образуется на фоне ишемии, гипертонии, стенозных патологий, миокардита, недостаточности клапана аорты.
Трапециевидная форма
В случае с конфигурацией в виде трапеции сердце теряет границы дуг, обретает тупость углов изгибов. К данной форме сердца могут привести заболевания сердечных камер, патологии миокарда, скопление в перикарде избыточной жидкости.
Методы оценки объема и формы сердца
Во время рентгенографического обследования межреберья сердечный объем рассчитывается по трем линиям на рентгенограмме бокового и переднего вида сердца. Однако данная методика позволяет получить только примерные показатели с погрешностью до 15 процентов.
Сегодня оценка сердечных объемов проводится зачастую при помощи ЭХО-КГ. Появление изменений в любой из камер сердца характеризуется своими особенностями.
При увеличении левого желудочка во время рентгенографии межреберья на переднем плане увеличивается длина оси данной части сердца, характеризующаяся тупостью углов.
Верхняя часть границы желудочка сердца опущена и округлена, при этом она нередко выходит за пределы границы ключиц.
Из-за увеличения размеров левого предсердия становится заметной выпуклость и удлинение контура третьей сердечной дуги с левой стороны. При существенном увеличении данной части сердца левое предсердие будет заступать на правую границу правого предсердия в межреберьи. Данная патология называется синдромом двойного контура.
Левым предсердием может быть сформирована еще одна лишняя дуга.
Внимание! Увеличенное левое предсердие в боковом виде на рентгенограмме показывает отклонение его к задней части пищевода. Изогнутая линия с небольшим радиусом – меньше 6 сантиметров и небольшой границы, свидетельствует о митральном стенозе
Если радиус изгиба и тупость его угла больше, это говорит о присутствии митральной недостаточности.