Диагностика миеломной болезни
Поставить диагноз бывает сложно, так как при миеломной болезни нет какой-то явной опухоли, которую можно заметить, а иногда заболевание вообще протекает без каких-либо симптомов.
Диагностикой миеломной болезни обычно занимается врач-гематолог. Во время расспроса врач выявляет основные симптомы заболевания у данного пациента, выясняет, нет ли кровотечений, боли в костях, частых простуд. Затем проводят дополнительные исследования, необходимые для точной постановки диагноза и определения стадии болезни.
-
Клинический анализ крови при миеломе часто указывает на увеличение вязкости крови и повышение скорости оседания эритроцитов (СОЭ). Нередко снижено количество тромбоцитов и эритроцитов, гемоглобина.
-
В результатах анализа крови на электролиты часто повышен уровень кальция; по данным биохимического анализа увеличено количество общего белка, определяются маркеры нарушения функции почек — высокие цифры мочевины, креатинина.
-
Анализ крови на парапротеин проводят для оценки типа и количества аномальных антител (парапротеинов).
-
В моче часто определяют патологический белок (белок Бенс-Джонса), который представляет собой моноклональные легкие цепи иммуноглобулинов.
-
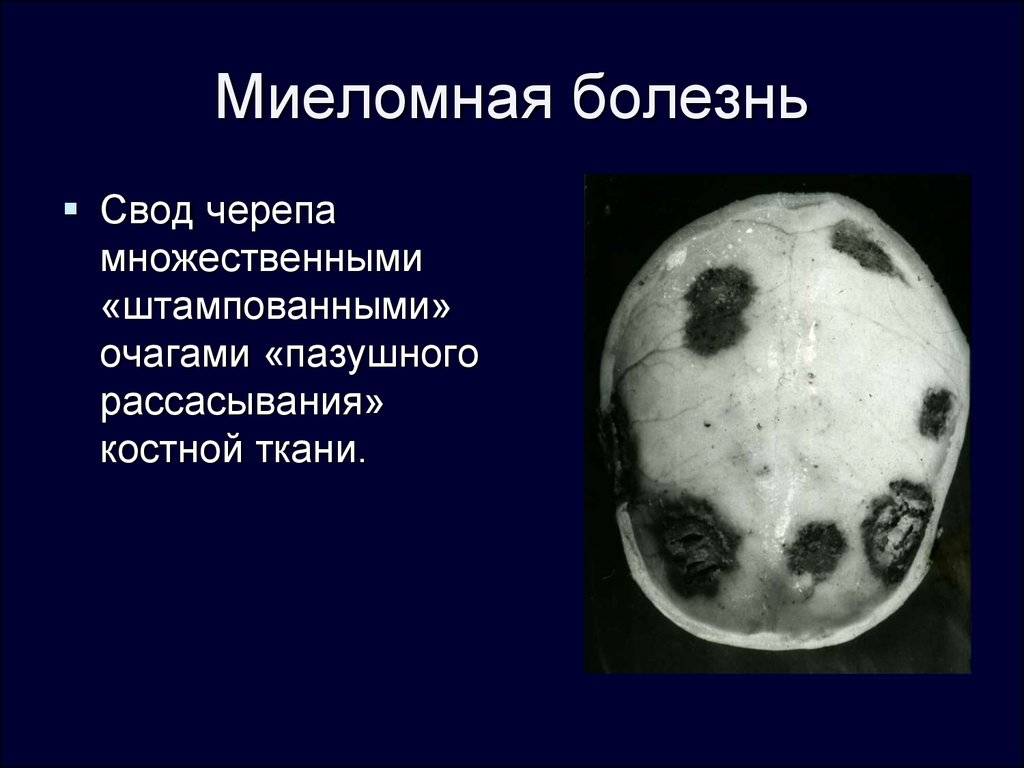
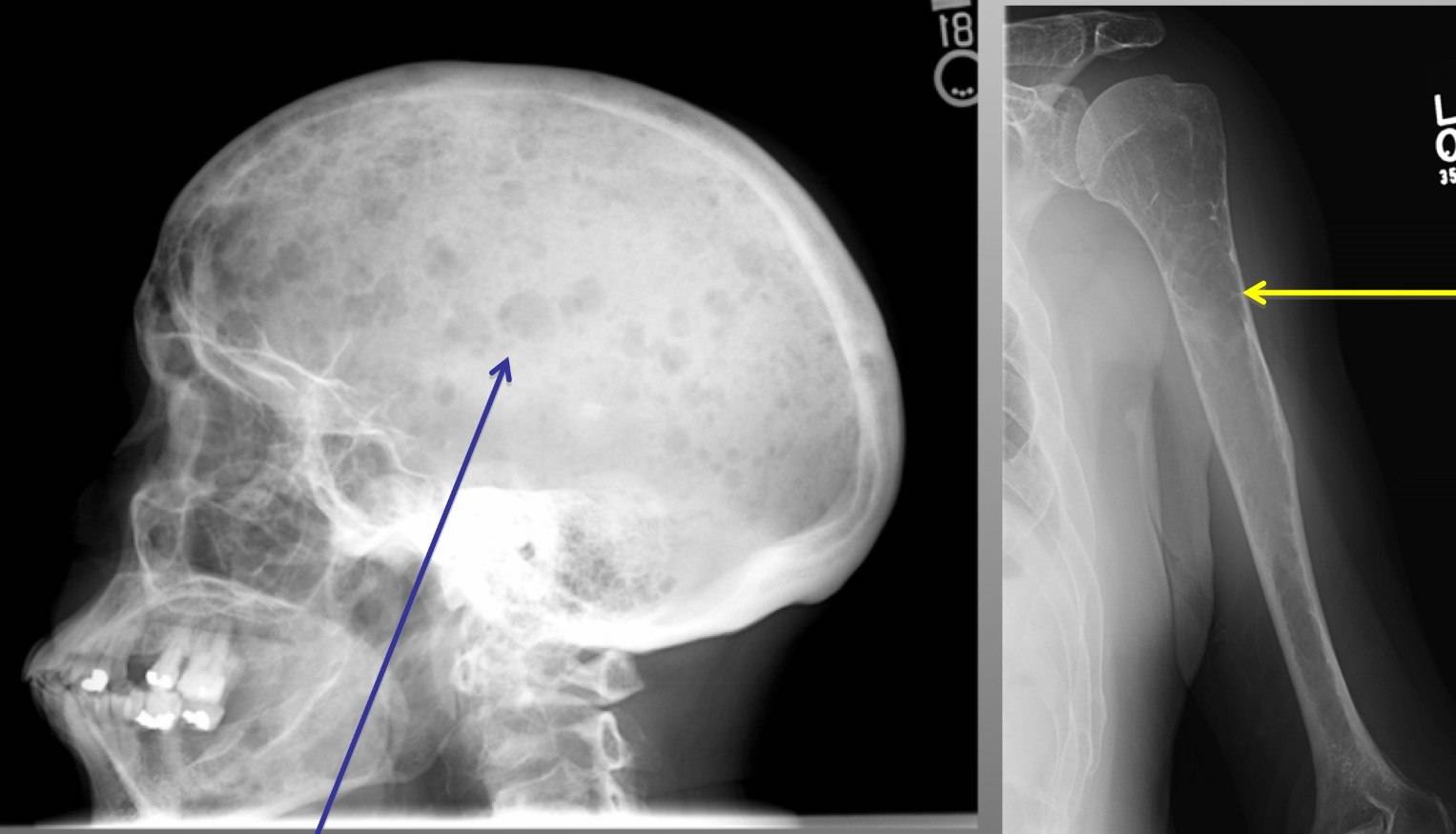
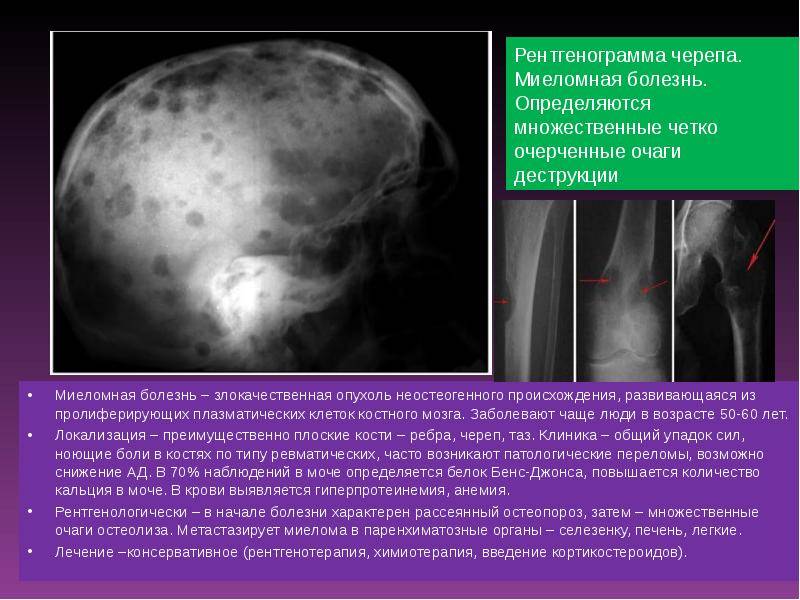
На рентгенограмме костей (черепа, позвоночника, бедренных и тазовых костей) видны характерные для миеломы повреждения.
-
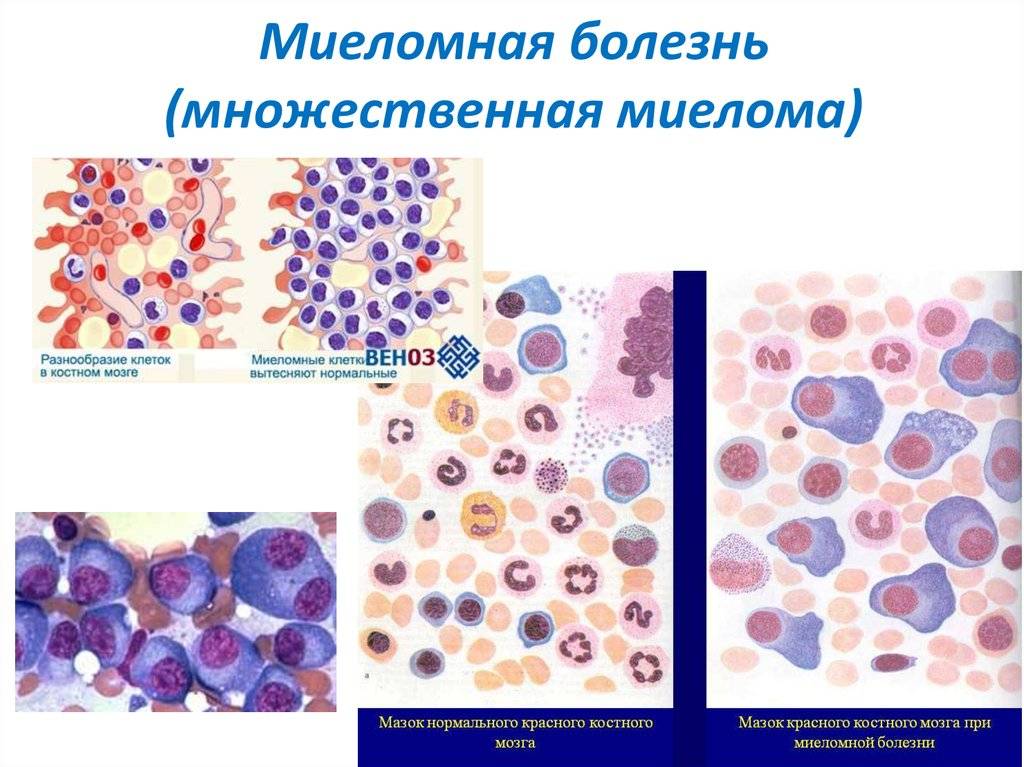
Пункция костного мозга — самый точный способ диагностики. Тонкой иглой берут кусочек костного мозга, обычно прокол делают в области грудины или кости таза. Затем полученный изучают под микроскопом в лаборатории на предмет перерожденных плазматических клеток и проводят цитогенетическое исследование для выявления изменений в хромосомах.
-
Компьютерная томография, магнитно-резонансная томография, ПЭТ-сканирование позволяют выявить участки повреждения в них.
Характеристика заболевания
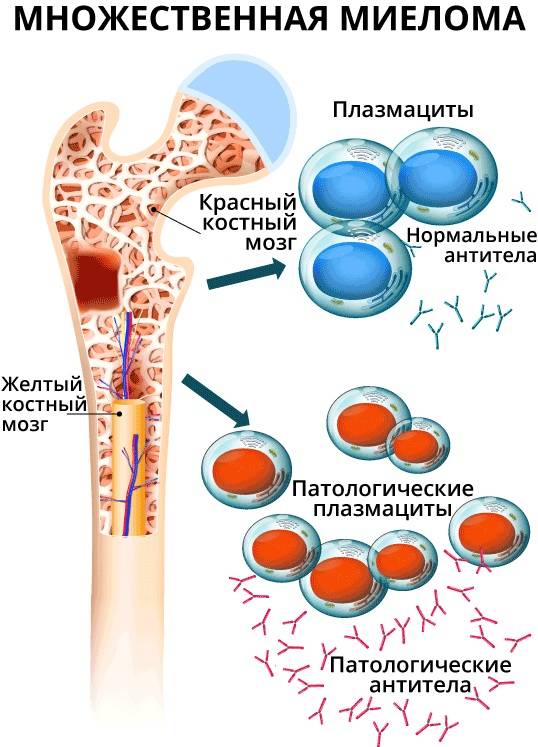
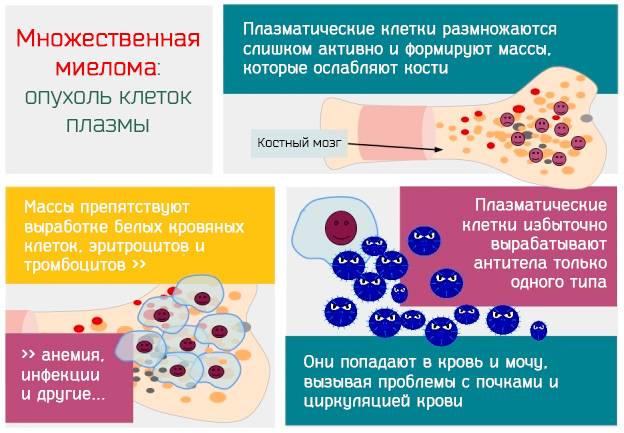
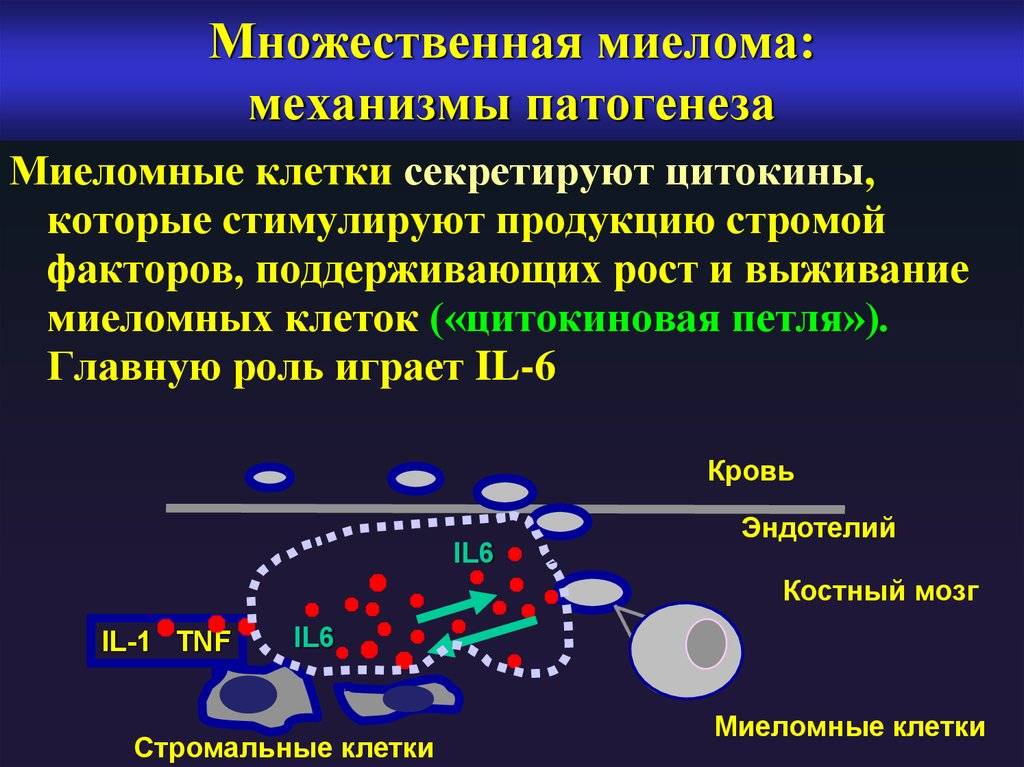
Миелома характеризуется злокачественным процессом активного разрастания в полости спинного мозга моноклональных плазмоцитов, продуцирующих патологический белок – парапротеин. Болезнь представляет собой непрекращающееся созревание и перерождение В-лимфоцитов в плазмоциты. Плазмоцит – это клетка, секретирующая иммуноглобулин. При миеломе моноклональные плазмоциты не погибают, а продолжают размножаться. Увеличение количества патогенов перемещается в костный мозг, что провоцирует снижение основных элементов крови.
Атипичные иммуноглобулины проникают в ткани других органов, накапливаясь в межклеточном пространстве. В первую очередь, патогены накапливаются в тканях почек, печени, селезенки и т.д. – органах с повышенным кровоснабжением.
Миеломная болезнь связана с замещением здоровых клеток атипичными иммуноглобулинами. Патогенез патологических плазмоцитов с выработкой биологически активных веществ вызывает развитие следующих эффектов:
- повышается уровень остеокластов, что провоцирует ломкость и хрупкость костей позвоночника, конечностей и т.д.;
- снижаются защитные функции организма;
- увеличивается уровень эластичных волокон с фиброгенами, что приводит к постоянному образованию капиллярных кровотечений и синяков;
- печёночные клетки активно разрастаются, провоцируя снижение свёртываемости крови;
- нарушенный белковый состав вызывает заболевания почек.
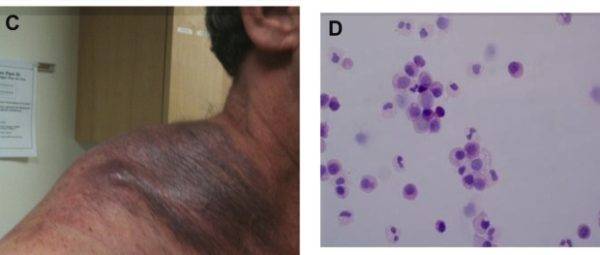 Проявления миеломы
Проявления миеломы
При миеломной болезни рост моноклональных плазмоцитов не контролируется и их уровень постоянно увеличивается. Из-за этого процесса миелома относится к злокачественным патологиям крови – гемобластозам.
Возникает заболевание обычно у взрослых людей после 40 лет. У мужчин болезнь диагностируется чаще, чем у женщин. Опухоль растёт медленно – до появления первых симптомов может пройти более 20 лет. После постановки диагноза, по наличию сопутствующей симптоматики человек живет в среднем в пределах 2 лет. Поэтому миелома часто воспринимается как рак крови.
Код по МКБ-10 у патологии С90 «Множественная миелома и злокачественные плазмоклеточные новообразования». Определить болезнь можно по наличию белков класса IgE, характеризуется присутствием Е-миеломы.
Диагностика
Критерии установления диагноза/состояния:
Критерии тлеющей (асимптоматической) ММ:
1. Моноклональный протеин:
- сыворотки крови ≥30 г/л и/или
- 500 мг в суточном анализе мочи и/или
- 10−59% клональных ПК в костном мозге.
2. Отсутствие органных повреждений и амилоидоза.
Симптоматическая ММ должна удовлетворять 3 критериям:
1. В костном мозге ≥10 % клональных ПК или верифицированная костная/экстрамедуллярная плазмоцитома + 1 симптом:
a) гиперкальциемия: кальций >11,5 мг/дл (>2,75 ммоль/л);b) дисфункция почек: креатинина крови >2 мг/дл (>173 ммоль/л), клиренсc) анемия: нормохромная нормоцитарная, Hb ниже нормы на 2 г/дл (20 г/л) илиd) 1 или более остеолитических очагов;e) клональных плазмоцитов в костном мозге >60 %;f) ненормальное соотношение свободных легких цепей (СЛЦ): ≥100 или ≤0,01;g)более 1 очага поражения костного мозга при МРТ.
2. Другие симптомы: гипервязкость, амилоидоз, >2 бактериальных инфекций за 12 мес.
Несекретирующая миелома:
- в пунктате костного мозга ≥10 % ПК,
- признаки CRAB-синдрома,
- при иммунофиксации в крови и моче нет моноклонального протеина,
- увеличение СЛЦ (2/3 пациентов).
2.2 Физикальное обследование
- визуальный терапевтический осмотр,
- терапевтические пальпация и аускультация,
- определение общего состояния по ECOG,
- осмотр миндалин и полости рта.
2.3 Лабораторные диагностические исследования
Лабораторные исследования:
- развернутый клинический анализ крови;
- общий (клинический) анализ мочи;
- количество белка в суточной моче;
- биохимический анализ крови;
- коагулограмма;
- клиренс креатинина;
- СКФ по СКD-EPI или MDRD.
Определение активности ММ или оценка ответа на терапию:
- электрофорез белковых фракций в крови (кроме несекретирующей, вялотекущей и миеломы легких цепей) и моче с количеством моноклонального и поликлональных иммуноглобулинов и β2-микроглобулина;
- иммунофиксация моноклональности иммуноглобулинов в крови и суточной моче с М-градиентом.
Определение СЛЦ в крови:
- несекретирующая ММ,
- олигосекретирующая ММ,
- вялотекущая миелома,
- миелома легких цепей,
- диализзависимая ХПН.
Для трансфузии определение:
- группы крови по AB0,
- антигена D системы Резус (резус-фактора),
- фенотипа антигенов эритроцитов.
Определение антител в крови:
- к вирусу гепатита C в крови;
- к поверхностному антигену (HBsAg) вируса гепатита B;
- классов M, G (IgM, IgG) к ВИЧ-1 и ВИЧ-2.
Уровень поликлональных иммуноглобулинов в крови для оценки гуморального иммунодефицита.
Стернальная пункция:
- миелограмма,
- иммунофенотипическое (проточная цитофлуориметрия) исследование мазка КМ.
Трепанобиопсия для ИГХ костного мозга.
Цитогенетика ПК (кариотипирование и FISH) для выявления прогностически важных аномалий:
- t(4;14),
- t(14;16),
- t(6;14),
- del 17p13,
- t(11;14),
- del13,
- плоидности и изменений хромосомы 1.
2.4 Инструментальные диагностические исследования
КТ:
- всех отделов позвоночника,
- грудной клетки,
- таза.
При невозможности КТ — рентгенологическое исследование костей.
Альтернатива КТ — ПЭТ/КТ.
МРТ всех отделов позвоночника и таза при подозрении
- на тлеющую миелому;
- на солитарную плазмоцитому;
- на компрессию спинного мозга.
При верифицированной ММ перед началом терапии:
- ЭКГ;
- эхо КГ;
- УЗ допплерография сосудов нижних конечностей;
- рентгенография или КТ органов грудной клетки;
- ЭГДС.
При коморбидности:
консультация соответствующего специалиста (кардиолога, невропатолога, ЛОР и др.)
Прогнозы, продолжительность жизни
Прогнозы дело неблагодарное, но существует определенная статистика, которую ведут крупные международные институты здравоохранения. Эта статистика говорит о том, что за последнее десятилетие общая выживаемость людей, больных множественной миеломой, увеличилась.
Успех лечения каждого пациента зависит от многих факторов:
- От возраста больного,
- От психологического состояния,
- От общего состояния организма,
- От эффективности выбранного лечения,
- От типа и стадии заболевания,
Хоть множественная миелома не поддается полному излечению, не стоит падать духом. В арсенале сегодняшней медицины имеется много способов лечения для того, чтоб остановить прогрессирование болезни. Больные люди получили шанс на продолжение жизни.
Диагностика спазма сосудов головного мозга
Проводя диагностику спазма сосудов головного мозга, врач обращает внимание на характерные симптомы и жалобы, наличие провоцирующих факторов и предрасположенности. Но для постановки окончательного диагноза врачу требуется проведение более тщательного обследования, которое включает в себя следующие методы:
- Рентген шейного отдела. С его помощью можно обнаружить характерные для остеохондроза изменения.
- УЗИ сосудов. Ультразвуковое исследование сосудов шеи позволяет узнать их диаметр, состояние, определить кровоток и ряд других важных параметров.
- МРТ. Это сложный, дорогостоящий и пока ещё не слишком распространенный метод диагностики дает весьма точную информацию о состоянии сосудов головного мозга.
Помимо этого могут потребоваться и другие методы диагностики, к примеру, биохимический анализ крови.
Способы лечения миеломной болезни
В настоящее время используют разные методы лечения, прежде всего лекарственную терапию, при которой препараты применяют в разных комбинациях.
-
Таргетная терапия с использованием лекарства (бортезомиб, карфилзомиб (не зарегистрирован в России), которые за счет влияния на синтез белков вызывают гибель плазматических клеток.
-
Терапия биологическими препаратами, такие как талидомид, леналидомид, помалидомид, стимулируют собственную иммунную систему бороться с опухолевыми клетками.
-
Химиотерапия циклофосфаном и мелфаланом, которые тормозят рост и приводят к гибели быстрорастущих клеток опухоли.
-
Кортикостероидная терапия (дополнительное лечение, которое усиливает эффект основных препаратов).
-
Бисфосфонаты (памидронат, золендроновая кислота) назначают для повышения плотности костной ткани.
-
Обезболивающие, в том числе наркотические анальгетики, применяют при сильных болях (очень частая жалоба при миеломной болезни), для облегчения состояния пациента применяют хирургические методы и лучевая терапия.
Хирургическое лечение требуется, например, для фиксации позвонков с помощью пластин или других приспособлений, так как происходит разрушение костной ткани, в том числе позвоночника.
После проведения химиотерапии часто проводят пересадку костного мозга, при этом наиболее эффективной и безопасной является аутологичная трансплантация стволовых клеток костного мозга, Для осуществления этой процедуры проводят забор стволовых клеток красного костного мозга. затем назначают химиотерапию (как правило, высокими дозами противоопухолевых препаратов), которая уничтожает раковые клетки. После окончания полного курса лечения делают операцию по пересадке забранных ранее образцов, и в результате начинают расти нормальные клетки красного костного мозга.
Некоторые формы заболевания (прежде всего “тлеющая” меланома) не требуют срочного и активного лечения. Химиотерапия вызывает тяжелые побочные эффекты и в некоторых случаях — осложнения, а эффекты на течение болезни и прогноз при бессимптомной “тлеющей” миеломной болезни сомнителен. В таких случаях проводят регулярное обследование и при первых признаках обострения процесса начинают лечение
План контрольных исследований и регулярность их проведения врач устанавливает индивидуально для каждого пациента, и очень важно соблюдать эти сроки и все рекомендации врача
Краткая информация
1.1 Определение заболевания или состояния
Множественная миелома (ММ) или плазмоклеточная миелома (ВОЗ 2017 г.):
- В-клеточная злокачественная опухоль,
- морфологический субстрат — плазматические клетки,
- продуцирует моноклональный иммуноглобулин.
1.2 Этиология и патогенез заболевания или состояния
Ведущий патогенетический факт — длительная, хроническая антигенная стимуляция после:
- вирусных инфекций,
- хронических заболеваний,
- длительного воздействия токсических веществ,
- радиации.
Особенности ММ связаны с:
- перестройкой локусов генов тяжелой цепи иммуноглобулина (IGH),
- хромосомными делециями,
- мутациями соматических генов,
- хромосомной гипердиплоидией с участием нечетного числа хромосом.
Вариабельность течения обусловлена количеством разных генетических нарушений.
1.3 Эпидемиология заболевания или состояния
Заболеваемость ММ:
- 1% среди всех ЗНО,
- 10−15% всех опухолей кроветворной и лимфоидной тканей,
- менее 2% у пациентов моложе 40 лет.
В РФ в 2017г.:
- 2,78 на 100 тыс.,
- 4 075 заболевших,
- 2 587 умерли.
Средний возраст заболевших ≈70 лет.
1.5 Классификация заболевания или состояния
Плазмоклеточные опухоли:
- моноклональная гаммапатия неясного генеза (не Ig-M тип);
- моноклинальная гаммапатия неясного генеза с вовлечением легких цепей;
- плазмоклеточная (множественная) миелома;
- варианты плазмоклеточной миеломы:
- вялотекущая (асимптоматическая),
- несекретирующая,
- плазмоклеточный лейкоз;
- плазмоцитома.
Множественная миелома классифицируется по стадиям и факторам риска.
1.6 Клиническая картина заболевания или состояния
Клинические проявления ММ в значительной мере определяются инфильтрацией костного мозга ПК и органными повреждениями.
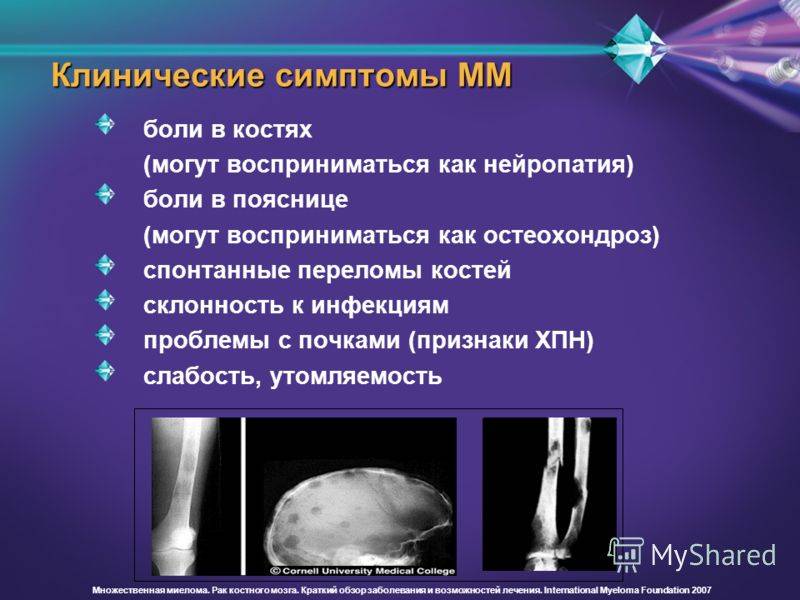
Симптомы костных повреждений:
- боль,
- переломы,
- компрессия спинного мозга,
- радикулярные боли.
Симптомы гиперкальциемии:
- полиурия,
- полидипсия,
- тошнота,
- рвота.
Симптомы почечной недостаточности:
- тошнота,
- рвота,
- недомогание,
- слабость.
Симптомы амилоидоза:
- периферическая нейропатия,
- отеки,
- органомегалия.
Симптомы инфильтрации миеломными клетками костного мозга:
- анемия,
- геморрагический синдром.
Симптомы снижения нормальных иммуноглобулинов:
- частые инфекции,
- пневмония.
Симптомы криоглобулинемии:
- синдром Рейно,
- акроцианоз.
Синдром гипервязкости:
- одышка,
- транзиторные ишемические атаки,
- тромбоз глубоких вен,
- кровоизлияния в сетчатку глаза,
- тромбоз центральной вены сетчатки или ее ветвей,
- носовые кровотечения.
Длительность заболевания до первых симптомов — от нескольких месяцев до ≥2−3 лет.
Миелома крови: какой прогноз и можно ли вылечиться?
Миелома крови представляет собой онкологическое заболевание, которое относят к парапротеинемическим лейкозам. Оно считается неизлечимым, однако поддается контролю, а правильно назначенное лечение позволяет добиться длительной ремиссии.
В каждом индивидуальном случае делается свой прогноз – можно ли вылечиться полностью или следует добиваться затухания процесса. Решение принимает только лечащий врач-онколог.
Что представляет собой миеломная болезнь
Заболевание имеет несколько названий – миеломная болезнь, множественная миелома, болезнь Рустицкого-Калера, секретирующая лимфома, генерализованная плазмоцитома.
К группе риска по миеломе относятся люди старшего возраста – от 60 лет и выше; мужчины болеют чаще женщин. Случаи миеломы у людей до 40 лет являются редкостью. По статистике, процент заболеваемости людей с черной кожей значительно выше, чем светлокожих.
Причиной болезни являются бесконтрольно продуцируемые костным мозгом плазматические клетки, которые скапливаются в костном мозге в виде плазмоцитом. В пораженных костных структурах мозг может полостью замещаться подобными атипичными клетками.
Сами злокачественные клетки при множественной миеломе не поступают в кровеносную систему, а вот парапротеины (видоизмененный иммуноглобулин), которые они вырабатывают, попадают в кровяное русло. Током крови их разносит по организму, они накапливаются в тканях организма и препятствуют работе всех органов.
Последствия роста плазматических клеток

- нарушение процесса кроветворения в тканях костного мозга;
- разрушение костей скелета;
- рост вязкости крови в связи с присутствием в ней большого количества парапротеинов;
- снижение иммунитета из-за уменьшения числа иммуноглобулинов;
- поражение почек в связи с оседанием в клубочках и почечных канальцах атипичных белков.
Клиническая картина болезни
Как и большинство злокачественных процессов, плазмацитома длительное время развивается бессимптомно.
Первыми признаками являются следующие проявления:
- болевые ощущения в поясничной области, ребрах и других частях опорно-двигательного аппарата;
- высокое значении солей кальция в моче и крови;
- повышенное СОЭ крови;
- белок появляется в моче, что является признаком серьезного нарушения работы почек;
- слабость, одышка, боли в сердечной области, снижение зрения.
Признаки заболевания не являются характерными, и больные обращаются за врачебной помощью к специалистам совершенно иного профиля, чем надо
В результате теряется столь важное при лечении любой онкологии время
Кроме того, пациенты с болями суставах или нижнем отделе позвоночника обращаются к помощи мануальных терапевтов. А это является прямым противопоказанием: костная ткань находится в процессе разрушения и нагрузка может иметь пагубные последствия.
Как выявить онкопатологию
Прогноз болезни напрямую зависит от срока ее выявления. К сожалению, бессимптомное протекание начальной стадии, что характерно для всех онкологических заболеваний, позволяет выявить миелому только случайно, в процессе обращения в медицинское учреждение по другому поводу.
Анализ крови, полученный через гематологический анализатор, покажет в виде гистограммы распределение эритроцитов, лейкоцитов и эритроцитов к крови.
Подходы к лечению
Практически не лечится. Целью терапии является прекращение дальнейшего развития процесса, чтобы на как можно более длительный срок растянуть ремиссию.
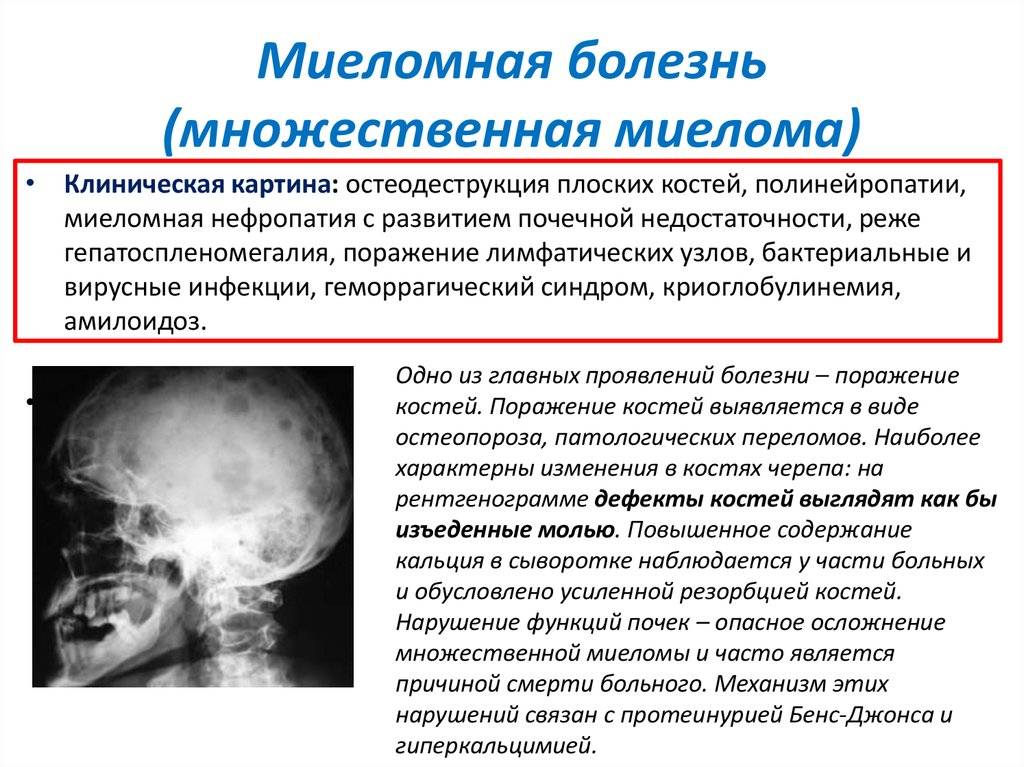
Поражение костей
Остеолитические разрушения костей являются центральным проявлением миеломной болезни и присутствуют у почти 80% пациентов во время установления диагноза. Генерализованное разрушение костей приводит к гиперкальциемии, ускоренному остеопорозу, формированию кифоза, клиновидным переломам позвонков. Стойкие изнурительные боли в костях являются ведущими жалобами, заставляющим больных впервые обратиться к врачу. К регулярным зонам поражения относится позвоночник и тазовые кости, что заканчивается переломами разных видов и возможной компрессией спинного мозга.
Доказано, что взаимодействие миеломных клеток с микроокружением в костном мозге приводит к выработке цитокинов, обуславливающих высокую активность остеокластов и пониженную деятельность остеобластов. Поэтому не обнаруживается признаков репарации кости в местах разрушений. Применение бифосфонатов, рентгенотерапии, балонной кифопластики и реконструктивной хирургии являются главными средствами реабилитации больных при разрушении костей. Однако костные разрушения сохраняются даже при излечении активной стадии болезни. Для выявления очагов остеолиза в костях скелета использую различные средства визуализации от рентгенографии всех костей и низкодозной комьютерной томографии до МРТ и ПЭТ всего тела. Наличие более одного фокуса лизиса в костях размером более 5 мм рассматривается как показание к назначению терапии для профилактики дальнейшего разрушения при отсутствии болевого синдрома.
Обязательной терапией деструкции и болевого синдрома при миеломной болезни в настоящее время является назначение бифосфонатов. Эти препараты были первоначально предложены для лечения остеопороза. Но они не только уменьшают боли, укрепляют кости, но также тормозят прогрессирование миеломной болезни. В связи с выделением через почки и длительной задержкой в организме бифосфонаты способны вызвать тяжелое поражение почек, простуду и гипокальциемию. Поэтому требуется мониторирования функции почек, а также электролитов (кальция и фосфора) при внутривенной терапии бифосфонатами.
Диагностика миеломной болезни
Лабораторная диагностика и скрининг парапротеинемий основан на выявлении «парапротеина» крови. Очень чувствительным методом диагностики парапротеинемий является иммунофиксация белков сыворотки и мочи с панелью антисывороток IgG, IgM, IgA, IgE, IgD, каппа, лямбда. Диагностическая значимость обнаружения парапротеинемии значительно увеличивается при характерной клинике, указывающей на плазмаклеточное заболевание. При скрининге лиц без симптомов методом электрофореза или иммунофиксации в отсутствии клинических проявлений миеломы обнаружение парапротеина указывают на моноклональную гаммапатию невыясненного значения (МГНЗ). К клиническим показаниям для исследования парапротеина относят боли в костях, патологические переломы, полинейропатию, лихорадку, анемию. Для парапротеинемий характерны такие лабораторные находки, как увеличение скорости оседания эритроцитов, протеинурия и азотемия, гиперкальцемия, увеличение содержания общего белка сыворотки, а также отклонения от нормы в содержании основных белковых фракций. Инфекционные процессы также часто сопутствуют миеломе, поскольку синтез парапротеина подавляет синтез нормальных иммуноглобулинов, что ведет к нарушению функций иммунной системы. Иммунохимическое исследование основных иммуноглобулинов сыворотки крови IgG, IgA, IgM позволяет выявить изменение их синтеза. Однако при оценке парапротеинемий иммунохимическое определение иммуноглобулинов не рекомендовано в связи с частым феноменом «прозоны» при высоких концентрациях и неточностью измерения моноклональных молекул, поскольку особенности синтеза в миеломной клетке меняют антигенные свойства иммуноглобулинов. Во всех этих случаях методом выбора для выявления и измерения парапротеина является электрофорез с иммунофиксацией белков сыворотки и мочи. Парапротеин представлен иммуноглобулином IgG примерно у половины больных, IgA — у 20%, IgD — у 2%, IgM — у 0.5%. У 20% больных парапротеин представлен только свободными цепями иммуноглобулина. В 2-3% случаев заболевания парапротеин не определяется, что рассматривается как несекретирующая миеломная болезнь. Если быть точным, это название не соответствует действительности, поскольку при несекретирующей миеломе можно обнаружить свободные легкие цепи в сыворотке крови или моче. Диагностическая панель из сочетания электрофореза сывороточного белка, сывороточной иммунофиксации и определения свободных легких цепей в сыворотке или электрофореза с иммунофиксацией в образце 24 часовой мочи рекомендована всем лицам с подозрением на миеломную болезнь. Чувствительность обнаружения моноклональных белков равняется в среднем 82% для электрофореза белков, 93% для иммунофиксации и 97% при добавлении результатов свободных легких цепей или электрофореза белка и иммунофиксации в образце 24-часовой мочи. Отсутствие моноклонального белка примерно у 2% больных типично для несекретирующей миеломной болезни.
В подавляющем числе случаев диагностика миеломной болезни начинается после появления характерной симптоматики. Диагноз миеломной болезни после появления таких симптомов, как повышенная утомляемость и боли в спине на практике обычно запаздывает на срок свыше 3 месяцев. Хотя неизвестно, как это сказывается на исходе заболевания в целом, но частота осложнений и госпитализаций за этот период отсрочки возрастает, что негативно влияет на качество жизни больных. Многие факторы влияют на причину задержки, включая неспецифический характер жалоб и расстройств, которые нередко наблюдаются у лиц пожилого возраста и которые первоначально рассматриваются ими и их родственниками как доброкачественные. Но устойчивый характер болей в позвоночнике и повышенной утомляемости должен всегда настораживать практических врачей. Обследование по поводу мышечно-скелетных болей, анемии, тромбоцитопении, почечной недостаточности, гиперкальциемии, неврологических расстройств может привести к обнаружению моклонального белка в сыворотке или моче.
Кроме того, диагностический поиск миеломной болезни включает полный подсчет клеток крови и СОЭ, измерение уровня сывороточного кальция и креатинина, электрофорез белков сыворотки и мочи с иммунофиксацией, исследование свободных легких цепей в крови, исследование пунктата костного мозга. Дополнительно, низко-дозная КТ всего тела или ПЭТ с 18-флюородезоксиглюкозой/ КТ или ,как минимум, обзорная рентенография всего скелета требуется для выявления остеолитических поражений костей.
Миеломная болезнь – лечение
В настоящее время для лечения миеломной болезни используется комплексный подход, с преимущественным применением лекарственных препаратов в различных комбинациях. Хирургическое лечение требуется для фиксации позвонков из-за их разрушения. Множественная миелома – лечение препаратами включает:
- таргетную терапию, стимулирующую синтез белков, ведущих борьбу с парапротеинами;
- химиотерапию, тормозящую рост раковых клеток и убивающую их;
- иммунную терапию, направленную на стимуляцию собственного иммунитета;
- кортикостероидную терапию, усиливающую основное лечение;
- лечение бисфосфонатами, укрепляющими костную ткань;
- обезболивающую терапию, направленную на снижение болевого синдрома.
Характеристика заболевания
Миеломатоз – самое распространённое заболевание в группе раковых опухолей плазматических клеток крови. Частота встречаемости миеломной болезни составляет до 1 % всех случаев онкологии и около 10 % случаев рака крови. Ежегодно среди 1 миллиона населения мира обнаруживается 30 новых случаев миеломы.
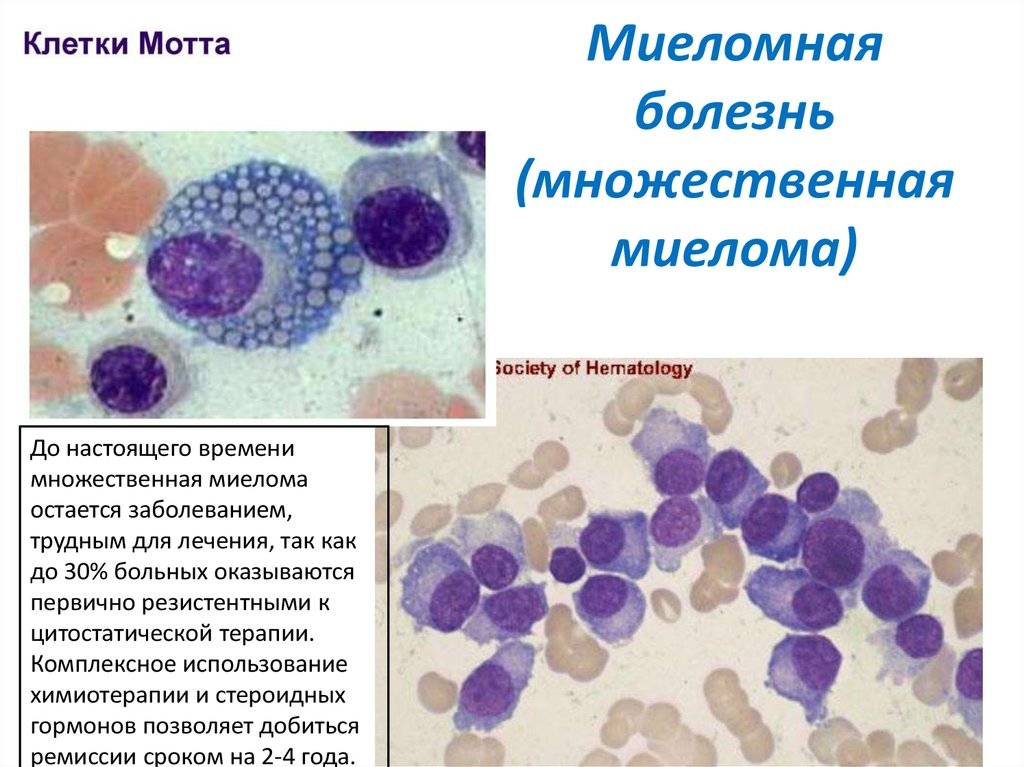
При данном виде онкологии происходит мутация одного из видов клеток крови – плазмоцитов. Плазмоциты или плазматические клетки – это конечная форма В-лимфоцитов. Их функция состоит в распознавании чужеродных агентов и выработке специфичных к ним антител (иммуноглобулинов).
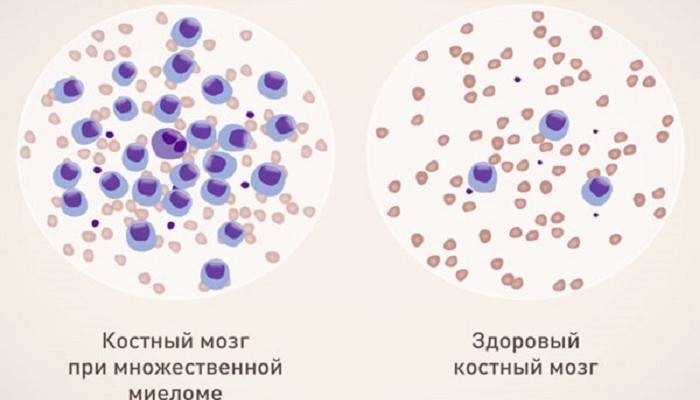
При мутации происходит патологическое размножение (пролиферация) одного из клонов плазматических клеток. Изменённые плазмоциты вырабатывают патологический иммуноглобулин – парапротеин, который является основным маркером миеломатоза при дифференциальной диагностике.
Болезни подвержены в основном пожилые пациенты, организм которых не в состоянии переносить тяжёлые интенсивные курсы химиотерапии. Поэтому срок между появлением первых мутировавших плазмоцитов и диагностикой заболевания непосредственно влияет на прогнозы выживаемости. При этом рост числа патологических клеток и развитие миеломной болезни могут происходить чрезвычайно медленно. От появления первых плазмоцитов с мутациями до образования очагов миеломы может проходить 20-30 лет.
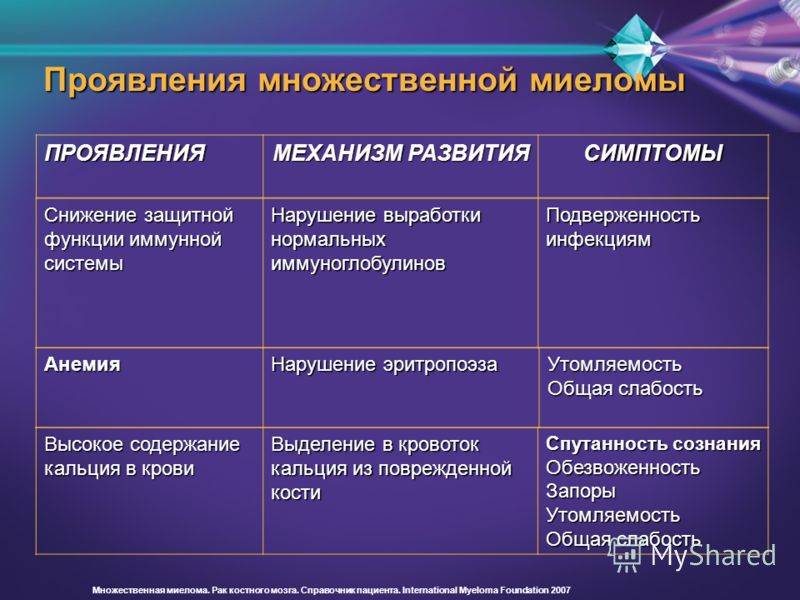
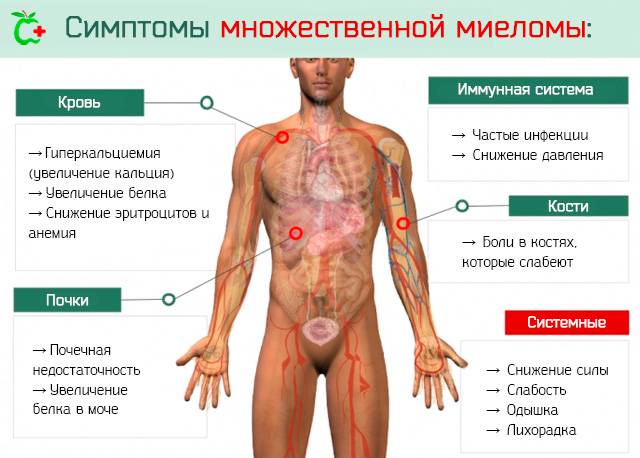
Миеломная болезнь – симптомы
Миеломная болезнь преимущественно возникает в пожилом возрасте, поражая как женщин, так и мужчин. Болезнь Рустицкого-Калера – симптомы и клиническая картина, наблюдаемая у заболевших:
- поражение кроветворной и костной систем;
- нарушение обменных процессов;
- патологические изменения в мочевыделительной системе.
Множественная миелома симптомы:
- самые первые признаки миеломной болезни – боль в костях (в позвоночнике, грудной клетке, костях черепа), спонтанные переломы, деформация костей и наличие опухолевых образований;
- частые пневмонии и другие заболевания, спровоцированные падением иммунитета и ограничением дыхательных движений, вызванным изменениями в костях грудной клетки;
- дистрофические изменения в мышцах сердца, сердечная недостаточность;
- увеличение селезенки и печени;
- миеломная нефропатия – нарушение в почках с характерным повышением белков в моче, переходящее в почечную недостаточность;
- нормохромная анемия – снижение количества эритроцитов и уровня гемоглобина;
- гиперкальциемия – повышенное количество кальция в плазме и в моче, это состояние очень опасно, его симптомы – рвота, тошнота, сонливость, нарушения работы вестибулярного аппарата, психические патологии;
- снижение уровня нормального иммуноглобулина;
- нарушения кроветворения – кровоточивость слизистых, появление синяков, спазмы артерий фаланг, геморрагический диатез;
- парестезии («мурашки»), головные боли, сонливость, переходящая в ступор, судороги, головокружения, глухота, одышка;
- на последних стадиях – снижение веса, повышение температуры тела, серьезная анемия.

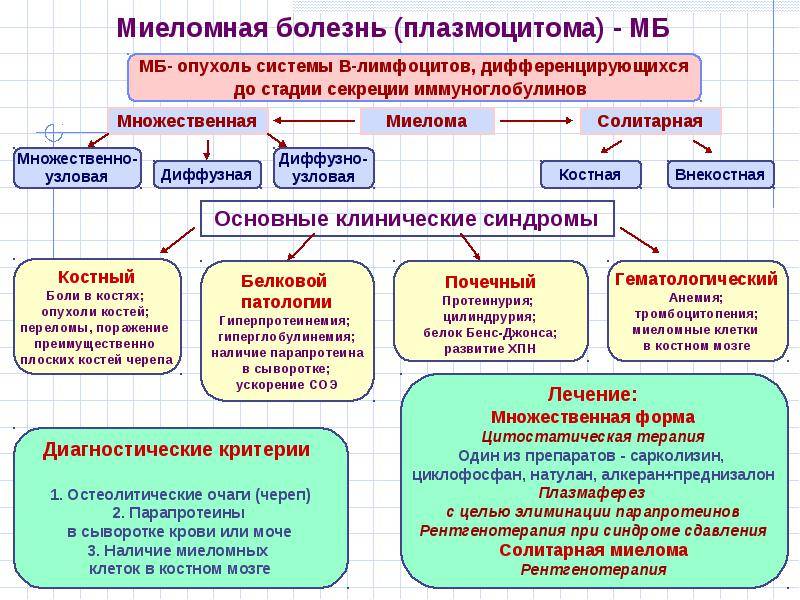
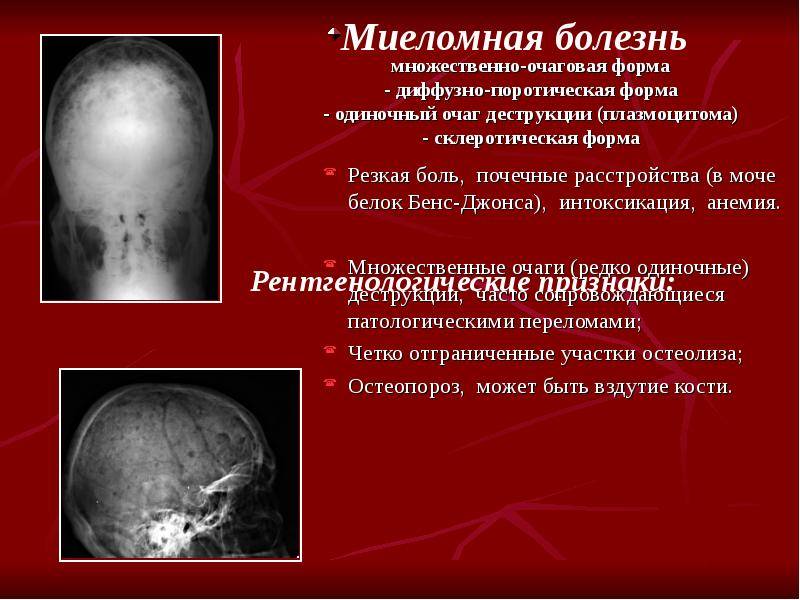
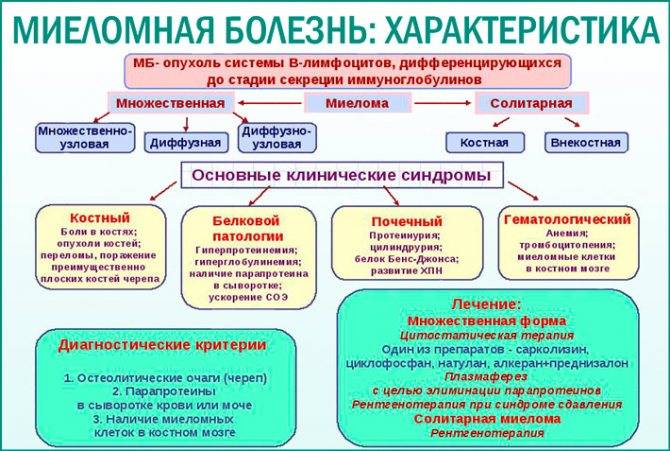
Формы миеломной болезни
По клинико-анатомической классификации миеломная болезнь бывает следующих форм:
- солитарная миелома – с одним опухолевым очагом в кости или лимфоузле;
- множественная (генерализованная) миелома – с формированием нескольких опухолевых очагов.
Кроме того, множественная миелома может быть:
- диффузной – в данном случае патологически образования не имеют границ, а пронизывают всю структуру костного мозга;
- множественно-очаговой – плазмоцитома кости развивается на ограниченных участках, а кроме этого, опухоли могут возникать в лимфатических узлах, селезенке.
- диффузно-очаговой – сочетающей признаки диффузной и множественной.
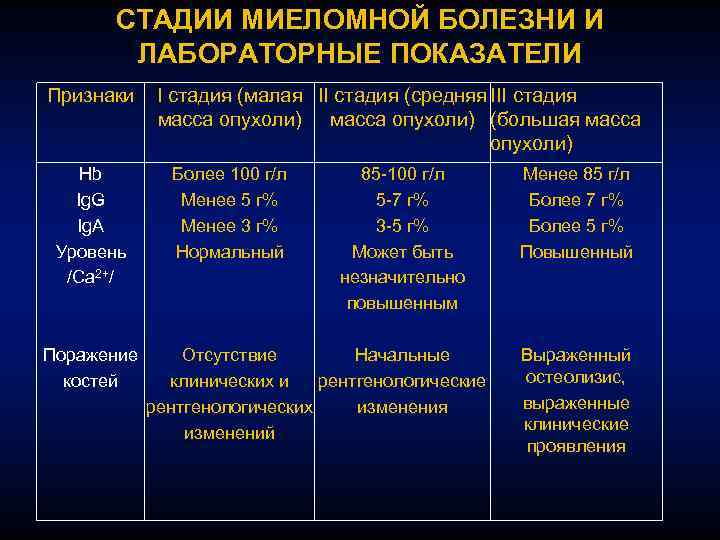
Миеломная болезнь – стадии
Врачи подразделяют три стадии множественной миеломы, вторая стадия является переходной, когда показатели выше, чем в первой, но ниже, чем в третьей (самой тяжелой):
- Первая стадия характеризуется – пониженным до 100 г/л гемоглобином, нормальным уровнем кальция, низкой концентрацией парапротеинов и белка Бенс-Джонса, одним опухолевым очагом размером 0,6 кг/м², отсутствием остеопороза, деформации костей.
- Третья стадия характеризуется – пониженным до 85 г/л и ниже гемоглобином, концентрацией кальция в крови выше 12 мг на 100 мл, множественными опухолями, высокой концентрацией парапротеинов и белка Бенс-Джонса, общим размером опухоли 1,2 кг/м² и более, явными признаками остеопороза.
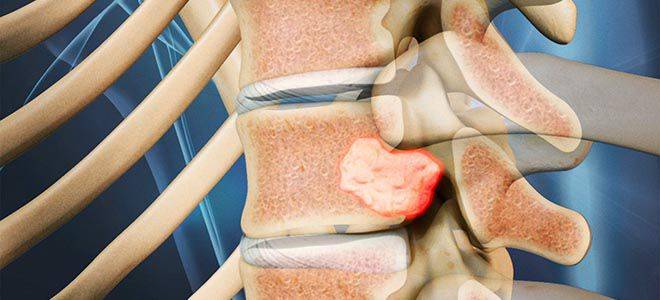
Осложнения миеломной болезни
Для множественной миеломы характерны осложнения, связанные с разрушающей деятельностью опухоли:
- сильные боли и разрушение костей (переломы);
- почечная недостаточность с необходимостью прохождения гемодиализа;
- постоянные инфекционные заболевания;
- анемия в серьезной стадии, требующая переливаний.
Лечение множественной миеломы
Одно и то же заболевание лечится разными препаратами и разными химиотерапевтическими схемами. Каждый пациент имеет свои индивидуальные особенности, возраст, стадию болезни, степень агрессивности и т.д. Основываясь на все эти факторы, врач подбирает лучшую схему для лечения каждого пациента.
Другим больным будет рекомендована только местная терапия, которая будет направлена на предотвращение инфекционных заболеваний, лечение анемии и уменьшение количества аномальных клеток.
Множественную миелому в сегодняшних онкологических больницах и центрах лечат с помощью:
- Химиотерапии. Данное заболевание лечат препаратами таргетного ряда. К нему относятся препараты Талидомид, Леналидомид и Бортезомид (Велкейд).
- Гормонотерапии.
- Трансплантации стволовых клеток.
Основной вид лечения, химиотерапия, имеет множество побочных эффектов (тошнота, рвота, падение лейкоцитов, облысение, нарушение в работе печени и почек, сердечные заболевания и др). Эти побочные эффекты частично снимаются сопроводительной терапией.
На основании специальных исследований определяется агрессивность миеломы. Соответственно, для таких форм заболевания понадобятся современные новые препараты.
Прогноз продолжительности жизни пациентов
Как уже говорилось выше, при миеломе крови прогноз выживаемости зависит от множества факторов.
Согласно данным специалистов в сфере онкологии, средняя продолжительность жизни после диагностирования миеломатоза не превышает года. Успешное лечение позволяет продлить этот срок в 2-5 раз в зависимости от стадии и формы болезни.

Например, применение терапии даже на третьей стадии миеломы, осложнённой поражением внутренних органов, позволяет увеличить продолжительность жизни пациента до 15 месяцев. Если болезнь протекает с меньшим количеством осложнений, то лечение позволяет продлить жизнь больного уже на 2,5 года. При I-II стадиях заболевания средняя продолжительность жизни после лечения составляет не менее 5 лет.
Интенсивная химиотерапия позволяет достичь частичной ремиссии более чем в 50 % клинических случаев миеломы.
Наибольшая продолжительность жизни достигается после успешной пересадки собственных или донорских периферических костномозговых клеток или при устранении очага солитарного миеломатоза. Длительность ремиссии в этом случае может составить 10 и более лет.
Прогноз лечения миеломной болезни во многом зависит от состояния здоровья больного. И в ещё большей степени – от стадии, на которой диагностирована патология. Поэтому периодическое прохождение обследования, особенно в случае наличия лейкоза в семейном анамнезе, полностью в интересах самого пациента.